题目内容
(1)有一种生产碘的方法是用亚硫酸氢钠还原碘酸盐(IO3-),每还原出1molI2,理论上需用去亚硫酸氢钠 moL.
(2)已知NaHS、MgSO4、NaHSO3组成的混和物中,硫元素的质量分数为a%,则混和物中氧元素的质量分数为
(3)在100ml含等物质的量的HBr和H2SO3的溶液中通入0.01摩尔Cl2,有一半Br-变为Br2(已知Br2能氧化H2SO3生成Br-和H2SO4),原溶液中HBr和H2SO3的浓度都等于 .
(2)已知NaHS、MgSO4、NaHSO3组成的混和物中,硫元素的质量分数为a%,则混和物中氧元素的质量分数为
(3)在100ml含等物质的量的HBr和H2SO3的溶液中通入0.01摩尔Cl2,有一半Br-变为Br2(已知Br2能氧化H2SO3生成Br-和H2SO4),原溶液中HBr和H2SO3的浓度都等于
考点:氧化还原反应的计算,元素质量分数的计算
专题:计算题
分析:(1)5HSO3-+2IO3-=3H++I2+5SO42-+H2O,根据碘和亚硫酸氢钠之间的关系式计算;
(2)NaHS、MgSO4、NaHSO3组成的混和物中,硫元素的质量分数为a%,Na和H元素的相对原子质量之和等于Mg元素的相对原子质量,根据硫和镁之间的关系式计算镁的质量分数,剩余部分为O元素的质量分数;
(3)Br2能氧化H2SO3,向含有HBr和H2SO3的溶液里通入氯气,氯气先和亚硫酸反应生成硫酸,然后氯气再和溴离子反应生成溴单质,根据氧化还原反应中得失电子守恒计算原溶液中HBr和H2CO3的浓度.
(2)NaHS、MgSO4、NaHSO3组成的混和物中,硫元素的质量分数为a%,Na和H元素的相对原子质量之和等于Mg元素的相对原子质量,根据硫和镁之间的关系式计算镁的质量分数,剩余部分为O元素的质量分数;
(3)Br2能氧化H2SO3,向含有HBr和H2SO3的溶液里通入氯气,氯气先和亚硫酸反应生成硫酸,然后氯气再和溴离子反应生成溴单质,根据氧化还原反应中得失电子守恒计算原溶液中HBr和H2CO3的浓度.
解答:
解:(1)5HSO3-+2IO3-=3H++I2+5SO42-+H2O,每还原出1molI2,理论上需用去亚硫酸氢钠物质的量=5mol,故答案为:5;
(2)NaHS、MgSO4、NaHSO3组成的混和物中,硫元素的质量分数为a%,Na和H元素的相对原子质量之和等于Mg元素的相对原子质量,根据硫和镁之间的关系式得镁的质量分数=
×24=0.75a%,剩余部分为O元素的质量分数,则O元素的质量分数=1-a%-0.75a%=1-1.75%,故答案为:1-1.75%;
(3)设亚硫酸和溴化氢的物质的量都为x.
氯气和溴化氢、亚硫酸反应的方程式分别为:Cl2+2HBr=Br2+2HCl、Cl2+H2SO3+H2O=H2SO4+2HCl,
由方程式知,反应中氯元素得电子的物质的量为0.01mol×2=0.02mol;
硫元素失电子的物质的量为x×(6-4)=2x,
溴元素失电子的物质的量为x×1×
=0.5x,
根据氧化还原反应中得失电子数相等得0.02mol=2x+0.5x,x=0.008mol,
所以原溶液中HBr和H2SO3的浓度都为
=0.08mol/L,
故答案为:0.08mol/L.
(2)NaHS、MgSO4、NaHSO3组成的混和物中,硫元素的质量分数为a%,Na和H元素的相对原子质量之和等于Mg元素的相对原子质量,根据硫和镁之间的关系式得镁的质量分数=
| a% |
| 32 |
(3)设亚硫酸和溴化氢的物质的量都为x.
氯气和溴化氢、亚硫酸反应的方程式分别为:Cl2+2HBr=Br2+2HCl、Cl2+H2SO3+H2O=H2SO4+2HCl,
由方程式知,反应中氯元素得电子的物质的量为0.01mol×2=0.02mol;
硫元素失电子的物质的量为x×(6-4)=2x,
溴元素失电子的物质的量为x×1×
| 1 |
| 2 |
根据氧化还原反应中得失电子数相等得0.02mol=2x+0.5x,x=0.008mol,
所以原溶液中HBr和H2SO3的浓度都为
| 0.008mol |
| 0.1L |
故答案为:0.08mol/L.
点评:本题考查了氧化还原反应的有关计算,(1)中正确书写方程式是解本题关键,结合物质之间的关系解答,(2)中注意等量代换,(3)中注意物质反应先后顺序,题目难度中等.

练习册系列答案
 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
下列说法中正确的是(NA表示阿伏加德罗常数的值)( )
| A、常温常压下,28g氮气所含有的原子数目为NA |
| B、1molNa被完全氧化生成Na2O2,失去电子数目为NA |
| C、标准状况下,22.4L水中含有NA个水分子 |
| D、1mol/L的CaCl2溶液中含有的Cl-数目为2NA |
下列过程中共价键被破坏的是( )
| A、碘升华 |
| B、食盐熔化 |
| C、水电解生成氢气和氧气 |
| D、水结成冰 |
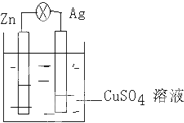 在银锌原电池中,以硫酸铜为电解质溶液,
在银锌原电池中,以硫酸铜为电解质溶液,