题目内容
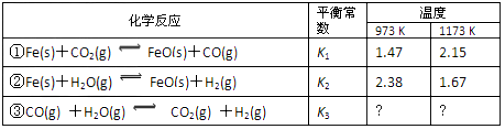
7.下列说法不正确的是( )| A. | 12C与14C为不同核素 | B. | 石墨和C60互为同素异形体 | ||
| C. | H2O和D2O互为同位素 | D. | ${\;}_{17}^{35}$X与${\;}_{17}^{37}$Y 为同种元素 |
分析 A.质子数和中子数一定的原子为元素的核素;
B.同种元素组成的不同单质为同分异构体;
C.质子数相同,中子数不同的同种元素的不同原子护卫同位素;
D.质子数相同的同类原子总称为元素;
解答 解:A.12C与14C具有一定质子数和中子数的原子为不同核素,故A正确;
B.石墨和C60是同种碳元素组成的不同单质,为同素异形体故B正确;
C.H2O和D2O是化合物,不能互为同位素,故C错误;
D.${\;}_{17}^{35}$X与${\;}_{17}^{37}$Y 质子数相同为同种元素,故D正确;
故选C.
点评 本题考查了原子结构、同位素、核素、同素异形体等的理解应用,掌握基础是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,即可构成CH4燃料电池.已知通入O2一极的电极反应式是:O2+2H2O+4e-═4OH-.下列有关叙述中,不正确的是( )
| A. | 通入CH4的电极为负极 | B. | 正极发生氧化反应 | ||
| C. | 溶液中的OH-向负极移动 | D. | 工作一段时间后应补充KOH |
18.固体NH4I在密闭容器中受热分解发生下列反应:NH4I(s)?NH3(g)+HI(g);2HI(g)?H2(g)+I2(g)达到平衡时,c(HI)=4mol/L,c(I2)=0.5mol/L,下列说法正确的是( )
| A. | 平衡时HI的分解率20% | B. | 反应起始时固体NH4I是5 mol | ||
| C. | 平衡时,c (NH3)=4.5mol/L | D. | 平衡时HI的分解率10% |
15.下列说法正确的是( )
①泥浆中泥沙是溶质,水是溶剂
②医用酒精中,水是溶剂,酒精是溶质
③凡是分散质能通过半透膜的分散系即属于胶体
④通过丁达尔现象可以鉴别胶体和溶液.
①泥浆中泥沙是溶质,水是溶剂
②医用酒精中,水是溶剂,酒精是溶质
③凡是分散质能通过半透膜的分散系即属于胶体
④通过丁达尔现象可以鉴别胶体和溶液.
| A. | ①②③④ | B. | ②④ | C. | ②③ | D. | ①②④ |
12.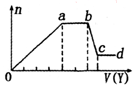 某无色稀溶液X中,可能含有如表所列离子中的某几种.取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(y)的关系如图所示.下列说法正确的是( )
某无色稀溶液X中,可能含有如表所列离子中的某几种.取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(y)的关系如图所示.下列说法正确的是( )
 某无色稀溶液X中,可能含有如表所列离子中的某几种.取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(y)的关系如图所示.下列说法正确的是( )
某无色稀溶液X中,可能含有如表所列离子中的某几种.取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(y)的关系如图所示.下列说法正确的是( )| 阴离子 | CO32-、SiO32-、[Al(OH)4]-、Cl- |
| 阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
| A. | 若Y是盐酸,则X中一定含有CO32-、SiO32-、[Al(OH)4]-和NH4+ | |
| B. | 若Y是NaOH溶液,则X中一定含有A13+、Fe3+、NH4+、Cl- | |
| C. | 若Y是NaOH溶液,则ab段发生反应的离子方程式为:NH4++OH-═NH3↑+H2O | |
| D. | 若Y是NaOH溶液,则X中的Al3+、Mg2+、NH4+物质的量之比为2:1:4 |
19.化学与生产、生活、科技等密切相关,下列说法正确的是( )
| A. | 石油裂解的目的是提高柴油等轻质油的产量和质量 | |
| B. | “神州七号”的防护层中含聚四氟乙烯,聚四氟乙烯属于不饱和烃 | |
| C. | 用CO2合成聚碳酸酯可降解塑料,可以实现“碳”的循环利用 | |
| D. | 煤经气化和液化两个化学变化过程,可变为清洁能源 |