题目内容
17.SiO2在自然界中广泛存在,它是制备现代通讯材料光导纤维(写该材料名称)的主要原料;以SiO2为原料,在工业上制备单质硅的化学方程式为SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;在常温下,SiO2可与一种酸发生反应,该反应的化学方程式为SiO2+4HF=SiF4↑+2H2O.该反应的重要应用是雕刻玻璃.分析 二氧化硅具有良好的光学特性,是制造光导纤维主要原料,二氧化硅能够与碳反应生成硅和一氧化碳,能够与氢氟酸反应生成四氟化硅和水,所以氢氟酸能腐蚀玻璃,可以用氢氟酸雕刻玻璃,据此解答;
解答 解:二氧化硅具有良好的光学特性,是制造光导纤维主要原料,二氧化硅能够与碳反应生成硅和一氧化碳,化学方程式:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,能够与氢氟酸反应生成四氟化硅和水,化学方程式:SiO2+4HF=SiF4↑+2H2O,所以氢氟酸能腐蚀玻璃,可以用氢氟酸雕刻玻璃;
故答案为:光导纤维;SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑;SiO2+4HF=SiF4↑+2H2O.
点评 本题考查化学方程式的书写,难度不大,注意把握硅和二氧化硅的性质,注意二氧化硅的用途,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.38.4g铜跟适量的浓硝酸反应,铜全部反应后,共收集到气体22.4L(标准状况),则反应消耗的HNO3的物质的量是( )
| A. | 2.2mol | B. | 1mol | C. | 1.6mol | D. | 2mol |
5.某无色混合气体中可能含有Cl2、SO2、NO、NO2、CO2 中的两种或多种气体.现将此无色的混合气体通过品红溶液后,品红溶液褪色,把剩余气体接触空气,很快变为红棕色.对于原混合气体成分的判断正确的是( )
| A. | 一定有NO2和Cl2 | B. | 一定有SO2 和NO | ||
| C. | 可能有NO2 | D. | 一定有SO2,可能有NO |
9.下列关于化学用语的表述正确的是(( )
| A. | 碳-14核素:${\;}_8^{14}C$ | B. | Ca2+的结构示意图为  | ||
| C. | 氮气的电子式 | D. | HCIO的结构式为H-Cl-O |
6.区别植物油和矿物油的正确方法是( )
| A. | 加水,振荡 | B. | 加Na0H溶液,煮沸 | C. | 加Na2SO4溶液 | D. | 直接观察 |
7.下列物质在空气里完全燃烧,生成二氧化碳和水的物质的量之比为1:1的有( )
| A. | 甲醇 | B. | 乙炔 | C. | 乙醇 | D. | 乙醛 |
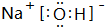 ;
;