题目内容
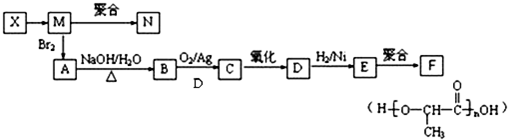
有机物A是最常用的食用油抗氧化剂,分子式为C10H12O5,可发生如下转化:

已知B的相对分子质量为60,分子中只含一个甲基.C的结构可表示为: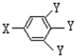 (其中:-X、-Y均为官能团)
(其中:-X、-Y均为官能团)
请回答下列问题:
(1)B的结构简式为 ;C中含有的官能团-X的名称为
(2)反应④的反应类型为 ;
(3)反应①的化学方程式为 ;
(4)从分子结构上看,A作为食用油抗氧化剂的主要原因是
a.含有苯环 b.含有羰基 c.含有酚羟基.

已知B的相对分子质量为60,分子中只含一个甲基.C的结构可表示为:
 (其中:-X、-Y均为官能团)
(其中:-X、-Y均为官能团)请回答下列问题:
(1)B的结构简式为
(2)反应④的反应类型为
(3)反应①的化学方程式为
(4)从分子结构上看,A作为食用油抗氧化剂的主要原因是
a.含有苯环 b.含有羰基 c.含有酚羟基.
考点:有机物的推断
专题:有机物的化学性质及推断
分析:A在氢氧化钠水溶液条件下发生水解反应,并酸化得到B与C,则A中含有酯基,其中B的相对分子质量为60,分子中只含一个甲基,能在浓硫酸的作用下发生消去反应,则B为CH3CH2CH2OH,发生消去反应得到D为CH3CH═CH2,D发生加聚反应得到高分子化合物E为 ,C能与碳酸氢钠溶液反应得到气体,则C含有-COOH,能与氯化铁溶液发生显色反应,则C中含有酚羟基,C的结构可表示为
,C能与碳酸氢钠溶液反应得到气体,则C含有-COOH,能与氯化铁溶液发生显色反应,则C中含有酚羟基,C的结构可表示为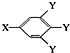 (其中:-X、-Y均为官能团),则C为
(其中:-X、-Y均为官能团),则C为 ,可推知A为
,可推知A为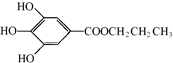 ,据此解答.
,据此解答.
 ,C能与碳酸氢钠溶液反应得到气体,则C含有-COOH,能与氯化铁溶液发生显色反应,则C中含有酚羟基,C的结构可表示为
,C能与碳酸氢钠溶液反应得到气体,则C含有-COOH,能与氯化铁溶液发生显色反应,则C中含有酚羟基,C的结构可表示为 (其中:-X、-Y均为官能团),则C为
(其中:-X、-Y均为官能团),则C为 ,可推知A为
,可推知A为 ,据此解答.
,据此解答.解答:
解:A在氢氧化钠水溶液条件下发生水解反应,并酸化得到B与C,则A中含有酯基,其中B的相对分子质量为60,分子中只含一个甲基,能在浓硫酸的作用下发生消去反应,则B为CH3CH2CH2OH,发生消去反应得到D为CH3CH═CH2,D发生加聚反应得到高分子化合物E为 ,C能与碳酸氢钠溶液反应得到气体,则C含有-COOH,能与氯化铁溶液发生显色反应,则C中含有酚羟基,C的结构可表示为
,C能与碳酸氢钠溶液反应得到气体,则C含有-COOH,能与氯化铁溶液发生显色反应,则C中含有酚羟基,C的结构可表示为 (其中:-X、-Y均为官能团),则C为
(其中:-X、-Y均为官能团),则C为 ,可推知A为
,可推知A为 ,
,
(1)由上述分析可知,B的结构简式为CH3CH2CH2OH,C为 ,官能团-X的名称为:羧基,故答案为:CH3CH2CH2OH;羧基;
,官能团-X的名称为:羧基,故答案为:CH3CH2CH2OH;羧基;
(2)反应④是CH3CH═CH2发生加聚反应得到高分子化合物 ,故答案为:加聚反应;
,故答案为:加聚反应;
(3)反应①的化学方程式为: ,
,
故答案为: ;
;
(4)由于苯酚在空气中易被氧化,A具有抗氧化作用的主要原因是分子中有酚羟基,故答案为:c.
 ,C能与碳酸氢钠溶液反应得到气体,则C含有-COOH,能与氯化铁溶液发生显色反应,则C中含有酚羟基,C的结构可表示为
,C能与碳酸氢钠溶液反应得到气体,则C含有-COOH,能与氯化铁溶液发生显色反应,则C中含有酚羟基,C的结构可表示为 (其中:-X、-Y均为官能团),则C为
(其中:-X、-Y均为官能团),则C为 ,可推知A为
,可推知A为 ,
,(1)由上述分析可知,B的结构简式为CH3CH2CH2OH,C为
 ,官能团-X的名称为:羧基,故答案为:CH3CH2CH2OH;羧基;
,官能团-X的名称为:羧基,故答案为:CH3CH2CH2OH;羧基;(2)反应④是CH3CH═CH2发生加聚反应得到高分子化合物
 ,故答案为:加聚反应;
,故答案为:加聚反应;(3)反应①的化学方程式为:
 ,
,故答案为:
 ;
;(4)由于苯酚在空气中易被氧化,A具有抗氧化作用的主要原因是分子中有酚羟基,故答案为:c.
点评:本题考查有机物的推断与合成,涉及酯、醇、羧酸、酚的性质与转化,注意根据B、C发生的系列反应,结合A发生的水解反应与分子式进行推断,是对有机物知识的总运用,理解酯类水解的原理是解题的关键,注意基础知识的掌握.

练习册系列答案
相关题目
氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为a HClO3=bO2↑+c Cl2↑+d HClO4+e H2O,用湿润的淀粉碘化钾试纸检验气体产物时,试纸先变蓝后褪色.下列说法正确的是( )
| A、由反应可确定:氧化性HClO4>HClO |
| B、变蓝的淀粉碘化钾试纸褪色是因为可能发生了:5C12+I2+6H2O=12H++10Cl-+2IO3- |
| C、若氯酸分解所得混合气体,lmol混合气体质量为47.6g,则反应方程式可表示:26HClO3=15O2↑+8C12↑+10HClO4+8H2O |
| D、若化学计量数a=8,b=3,则该反应转移电子数为10e- |
表示下列变化的化学用语正确的是( )
| A、NaHCO3的水解:HCO3-+H2O?H3O++CO32- | ||||
| B、1L 0.5mol?L-1稀硫酸与1L 1mol?L-1氢氧化钠溶液反应放出57.3kJ的热量:H2SO4(aq)+2NaOH(aq)═Na2SO4(aq)+2H2O(1);△H=-57.3 kJ/mol | ||||
| C、氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- | ||||
D、以惰性电极电解KCl溶液:2Cl-+2H2O
|