��Ŀ����
18������笠ƾ���[5Ca��NO3��2•NH4NO3•10H2O]��������ˮ����һ����ɫ�ĸ��Ϸ��ϣ���1������笠ƾ������Һ�����ԣ�ԭ����NH4++H2O?NH3•H2O+H+�������ӷ���ʽ��ʾ����
��2����ҵ����������笠Ƶķ������������ȡ��ʯ�õ��Ĵ�����ƣ�������ơ�����Ƽ����ᣩΪԭ���Ʊ�������������Ϊ��

����������Ҫ�ɷ���Ca3��PO4��2���ѧʽ����
�ڼ���������̼��ƺ�����Ӧ�����ӷ���ʽΪCaCO3+2H+�TCa2++CO2��+H2O��
���������һ���ֽ�����ʣ����������ʱ��������ڽϵ��¶ȣ�230��400��ʱ������ֽ�ɿ����к��������������壬�䷴Ӧ�Ļ�ѧ����ʽΪ2NH4NO3$\frac{\underline{\;230��400��\;}}{\;}$2N2��+O2��+4H2O��
��3����������笠ƹ����ķ�ˮ�г���������泥���ͳ�ľ��������Ƿ�������������
��NO${\;}_{2}^{-}$�����������¿�ת��ΪN2���÷������������ð뷴Ӧ��ͬ�缫��Ӧʽ����ʾ2NO3-+10e-+12H+�T6H2O+N2����
��Ŀǰ���õ�ⷨ����������ԭ����ͼ��ʾ����Ĥ����Ĥ�ֱ�ֻ���������ӡ�������ͨ������

�������ĵ缫��ӦΪ2H2O-4e-�T4H++O2�������ҿɻ��յIJ�ƷΪ���ᣨ�����ƣ���
���ҿɻ��յ�������ԭ��Ϊ���ʱ�����������ӵõ��ӷ�����ԭ��Ӧʹ������ǿ�����������ƶ���笠����ӷ�Ӧ���ɰ�����
���� ��1��笠�����ˮ�������ԣ�
��2��������ƣ�������ơ������P���ᣩ��ˮ�ܽ⣬���˵ú�����ƺ��������Һ������̼��������ᷴӦ��������ơ�ˮ�Ͷ�����̼���壬��ͨ�백���к�������������泥��������õ���ҺΪ����ƺ�����淋Ļ����Һ�������ᾧ�õ�����笠�[5Ca��NO3��2•NH4NO3•10H2O]���壬�ݴ˷������
��3���ٷ�����������ijЩϸ�������������½�NO3-�õ����ӷ�����ԭ��Ӧ����N2���ݴ���д��
�ڸ���Ĥ��ⷨ������Ϊˮʧ���ӷ�����������Ӧ��������������������ʹ������ǿ�����������ƶ����������ϳ����
�۵��ʱ������Ϊ����ӦΪ�����ӵõ��ӷ�����ԭ��Ӧ������������ʹ������ǿ�����������ƶ���笠����ӷ�Ӧ���ɰ������ݴ˷�����
��� �⣺��1��笠�����ˮ�������ԣ���ˮ�����ӷ�ӦΪNH4++H2O?NH3•H2O+H+���ʴ�Ϊ��NH4++H2O?NH3•H2O+H+��
��2���������Ϊ������ˮ�����ʣ�����������Ҫ�ɷ�������ƣ���ѧʽΪ��Ca3��PO4��2���ʴ�Ϊ��Ca3��PO4��2��
�ڼ���̼��������ᷴӦ��������ơ�ˮ�Ͷ�����̼���壬������Ӧ�����ӷ���ʽΪCaCO3+2H+�TCa2++CO2��+H2O���ʴ�Ϊ��CaCO3+2H+�TCa2++CO2��+H2O��
�ۿ����к���������������ֱ��ǵ���������������������ԭ��Ӧԭ���ó�����立ֽⷽ��ʽΪ��2NH4NO3$\frac{\underline{\;230��400��\;}}{\;}$2N2��+O2��+4H2O���ʴ�Ϊ��2NH4NO3$\frac{\underline{\;230��400��\;}}{\;}$2N2��+O2��+4H2O��
��3���ٷ�����������ijЩϸ�������������½�NO3-ת��ΪN2����NO3-�õ����ӷ�����ԭ��Ӧ����N2����ӦʽΪ2NO3-+10e-+12H+�T6H2O+N2�����ʴ�Ϊ��2NO3-+10e-+12H+�T6H2O+N2����
��Ĥ��ⷨ������Ϊˮʧ���ӷ�����������Ӧ����ӦʽΪ2H2O-4e-�T4H++O2���������������������������ʹ������ǿ�����������ƶ����������ϳ����ᣬ���Ԣ��ҿɻ��յIJ�ƷΪ����ʴ�Ϊ��2H2O-4e-�T4H++O2�������
�۵��ʱ������Ϊ����ӦΪ�����ӵõ��ӷ�����ԭ��Ӧ��������������ʹ������ǿ�����������ƶ���笠����ӷ�Ӧ���ɰ��������Ԣ��ҿɻ��յ�������
�ʴ�Ϊ�����ʱ�����������ӵõ��ӷ�����ԭ��Ӧʹ������ǿ�����������ƶ���笠����ӷ�Ӧ���ɰ�����
���� ������Ҫ�����˹�ҵ��������笠Ƶ�ԭ������ˮ�Ĵ��������ڿ��鿼���Ķ�����Ϣ����������������������װ�õķ�������缫��Ӧʽ����д���״��㣬�ѶȽϴ�

 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д�| A�� | ������ԭ�ӹ��ɵ����ʲ�һ�����ڻ����� | |
| B�� | ����һ��Ԫ�ص�����һ��Ϊ������ | |
| C�� | ���ܺ������ܺͼ����Ӧ��������һ��Ϊ���������� | |
| D�� | �Ⱥ��н���Ԫ���ֺ��зǽ���Ԫ�صĻ�����һ��Ϊ���ӻ����� |
| A�� | ������Ϊ37����ԭ��${\;}_{37}^{17}$Cl | B�� | ��ԭ�ӵĵ���ʽ | ||
| C�� | ��ԭ�ӵĽṹʾ��ͼ | D�� | �����ӵĽṹʾ��ͼ |
| A�� | ETFE�Ľṹ�У�����-CF2-CH2-CF2-CH2-���ӷ�ʽ | |
| B�� | �ķ���ϩ����ϩ�������۷�Ӧ�õ�ETFE | |
| C�� | ����ϩΪԭ�Ͼ����ӳɷ�Ӧ��ȡ����Ӧ���Ƶ��Ҷ��� | |
| D�� | ETFE�������ȹ��ͣ����νṹ�������� |
 X��Y��Z��W��Ϊ������Ԫ�أ�������Ԫ�����ڱ������λ����ͼ��ʾ����Zԭ�ӵ������������ǵ�һ���������3��������˵����ȷ���ǣ�������
X��Y��Z��W��Ϊ������Ԫ�أ�������Ԫ�����ڱ������λ����ͼ��ʾ����Zԭ�ӵ������������ǵ�һ���������3��������˵����ȷ���ǣ�������| A�� | Z������������Ӧ��Y���� | |
| B�� | ����������Ӧˮ��������W��Zǿ | |
| C�� | X����������ǿ��Y���� | |
| D�� | X��W��ԭ�Ӻ�����������9 |
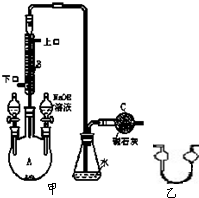 �Ʊ��屽��ʵ��װ����ͼ��ʾ���ش��������⣺
�Ʊ��屽��ʵ��װ����ͼ��ʾ���ش��������⣺ ��ͼ��Ԫ�����ڱ��и����壨A��������IJ���Ԫ�ط��Ŵ��루��Ӱ��Ϊ��������
��ͼ��Ԫ�����ڱ��и����壨A��������IJ���Ԫ�ط��Ŵ��루��Ӱ��Ϊ��������