题目内容
6.1mol单质A投入到足量的浓硝酸中,在一定条件下发生反应,耗掉硝酸4mol,则组成单质A的元素在反应后的化合价可为( )①+1 ②+2 ③+3 ④+4.
| A. | ①或② | B. | ①或④ | C. | ②或③ | D. | ②或④ |
分析 若A为金属单质,A为+1价金属,则1mol单质A与浓硝酸反应生成1molNO2和1mol硝酸盐;A为+2价金属,则1mol单质A与浓硝酸反应生成2molNO2和1mol硝酸盐;
A为+3价金属,则1mol单质A与浓硝酸反应生成3molNO2和1mol硝酸盐;
若A为非金属单质,如单质碳,则1mol单质A与浓硝酸反应生成4molNO2,结合原子守恒分析.
解答 解:若A为金属单质,A为+1价金属,则1mol单质A与浓硝酸反应生成1molNO2和1mol硝酸盐,所以消耗的硝酸为2mol,与题意不符;
A为+2价金属,则1mol单质A与浓硝酸反应生成2molNO2和1molA(NO3)2,所以消耗的硝酸为4mol,与题意相符;
A为+3价金属,则1mol单质A与浓硝酸反应生成3molNO2和1molA(NO3)3,所以消耗的硝酸为6mol,与题意不符;
若A为非金属单质,如单质碳,则1mol单质A与浓硝酸反应生成4molNO2,反应消耗4mol硝酸,与题意相符;
综上可知组成单质A的元素在反应后的化合价可为+2或+4;
故选D.
点评 本题考查了有关硝酸的计算,题目难度中等,注意把握反应产物的判断结合原子守恒和得失电子守恒计算,侧重于考查学生的分析能力和计算能力.

练习册系列答案
相关题目
13.波尔多液是果农常用的一种杀菌剂,氯吡苯脲是一种西瓜膨大剂(植物生长调节剂),其组成结构和物理性质见表.
回答下列问题:
(1)氯吡苯脲晶体中,氮原子的杂化轨道类型为sp3、sp2杂化.
(2)氯吡苯脲晶体中,微粒间的作用力类型有BCD.
A.离子键 B.极性键 C.非极性键 D.配位键 E.氢键.
| 分子式 | 结构简式 | 外观 | 熔点 | 溶解性 |
| C12H10ClN3O |  | 白色结晶粉末 | 170~ 172℃ | 易溶 于水 |
(1)氯吡苯脲晶体中,氮原子的杂化轨道类型为sp3、sp2杂化.
(2)氯吡苯脲晶体中,微粒间的作用力类型有BCD.
A.离子键 B.极性键 C.非极性键 D.配位键 E.氢键.
11.将一定质量的锌片放入500mLCuSO4溶液中,二者恰好完全反应,待充分反应后取出锌片,洗净后称量,发现锌片比原来减轻了0.5g,则该CuSO4溶液的物质的量浓度为( )
| A. | 0.5mol•L-1 | B. | 1mol•L-1 | C. | 1.5mol•L-1 | D. | 2mol•L-1 |
18. 常温下,实验测得1.0mol/L NH4HCO3溶液pH=8.0.平衡时碳的分布系数(各含碳微粒的浓度占含碳各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( )
常温下,实验测得1.0mol/L NH4HCO3溶液pH=8.0.平衡时碳的分布系数(各含碳微粒的浓度占含碳各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( )
 常温下,实验测得1.0mol/L NH4HCO3溶液pH=8.0.平衡时碳的分布系数(各含碳微粒的浓度占含碳各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( )
常温下,实验测得1.0mol/L NH4HCO3溶液pH=8.0.平衡时碳的分布系数(各含碳微粒的浓度占含碳各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( )| A. | 常温下ka(H2CO3)>Kb(NH3•H2O)>Ka2(H2CO3) | |
| B. | pH=13时,溶液中不存在HC03-的水解平衡 | |
| C. | pH由8~11时,$\frac{(C{O}_{3}^{2-})•c({H}^{+})}{c(HC{O}_{3}^{-})}$不变 | |
| D. | pH=3时,有c(NH4+)+c(NH3•H2O)═c(HCO3-)+c(CO32-)+c(H2CO3) |
15.氢氧化钠晶体熔化的过程中,破杯了( )
| A. | 共价键和离子键 | B. | 离子键 | C. | 离子键和金属键 | D. | 共价键 |
16.有关实验叙述不正确的是( )
| A. | 滴定管、容量瓶和分液漏斗使用前都要检漏、干燥 | |
| B. | 滴定管没有用标准液润洗,会导致测定结果偏高 | |
| C. | 滴定管中加标准液后,要调节液面位置在零刻度或以下 | |
| D. | 胆矾结晶水含量测定时,需用小火缓慢加热,防止晶体飞溅 |
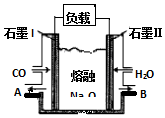
 汽车作为一种现代交通工具正在进入千家万户,汽车尾气中含有CO、NO2等有毒气体,其污染问题也成为当今社会急需解决的问题.
汽车作为一种现代交通工具正在进入千家万户,汽车尾气中含有CO、NO2等有毒气体,其污染问题也成为当今社会急需解决的问题.