题目内容
7.提纯含有少量泥沙的粗盐,下列操作顺序正确的是( )| A. | 过滤、蒸发、结晶、溶解 | B. | 溶解、蒸发、结晶、过滤 | ||
| C. | 溶解、蒸发、过滤、结晶 | D. | 溶解、过滤、蒸发、结晶 |
分析 提纯含有少量泥沙的粗盐,先将固体溶于水形成溶液,再将泥沙通过过滤的方法除去,得到氯化钠溶液,再从氯化钠溶液中获得氯化钠固体,据此分析.
解答 解:提纯含有少量泥沙的粗盐,先将固体溶于水形成溶液,过滤除去泥沙,将滤液进行蒸发、结晶获得氯化钠固体,所以操作顺序为溶解、过滤、蒸发、结晶,故选D.
点评 本题主要考查物质的分离提纯,应注意的是实验基本操作的灵活运用,难度不大.

练习册系列答案
相关题目
12.从化学反应速率和化学平衡两方面去考虑,工业合成氨反应:N2(g)+3H2(g)?2NH3(g)△H<0应采用的适宜条件是( )
| A. | 低温、高压、催化剂 | B. | 低温、低压、催化剂 | ||
| C. | 高温、高压、催化剂 | D. | 适宜温度、高压、催化剂 |
16.将绿矾(FeSO4•7H2O)、硫酸铵[(NH4)2SO4]以相等物质的量混合可制得摩尔盐[FeSO4•(NH4)2SO4•6H2O]晶体.

I.根据上图回答:
(1)步骤1中加入Na2CO3溶液的作用洗涤铁屑表面的油污.结合离子方程式简要说明步骤1中加热的原因CO32-+H2O?HCO3-+OH-,加热促进CO32-的水解,增大OH-浓度.
(2)制得的晶体过滤后用无水乙醇洗涤而不用蒸馏水,理由是摩尔盐易溶于水而难溶于乙醇.
Ⅱ.制摩尔盐的原料之一是硫酸铵,评价硫酸铵化肥的主要指标如下:
某研究性学习小组对某硫酸铵化肥样品进行了如下实验探究:

【观察外观】该硫酸铵化肥无可见机械杂质.
【实验探究】按图示装置进行实验.
【交流讨论】
(1)甲同学:根据此实验测得的数据,计算的硫酸铵化肥的含氮量偏高(填偏高、偏低、或不影响),实验装置中存在一个明显缺陷是缺少干燥装置.
(2)乙同学:实验过程中,往烧瓶中加入的浓氢氧化钠溶液一定要足量并充分加热,原因是NH4++OH-═NH3↑+H2O,使得NH4+全部转化为NH3,最终进入B装置被吸收.
【探究结论】
(3)称取27.0g硫酸铵化肥样品,用改进后的实验装置重新进行实验,测得实验后B装置增重6.8g.则该化肥含氮量为20.7%,由此可判断该化肥的品质.

I.根据上图回答:
(1)步骤1中加入Na2CO3溶液的作用洗涤铁屑表面的油污.结合离子方程式简要说明步骤1中加热的原因CO32-+H2O?HCO3-+OH-,加热促进CO32-的水解,增大OH-浓度.
(2)制得的晶体过滤后用无水乙醇洗涤而不用蒸馏水,理由是摩尔盐易溶于水而难溶于乙醇.
Ⅱ.制摩尔盐的原料之一是硫酸铵,评价硫酸铵化肥的主要指标如下:
| 优等品 | 一等品 | 合格品 | |
| 外观 | 白色结晶,无可见机械杂质 | 无可见机械杂质 | |
| 氮(N)含量 | ≥21.0% | ≥21.0% | ≥20.5% |

【观察外观】该硫酸铵化肥无可见机械杂质.
【实验探究】按图示装置进行实验.
【交流讨论】
(1)甲同学:根据此实验测得的数据,计算的硫酸铵化肥的含氮量偏高(填偏高、偏低、或不影响),实验装置中存在一个明显缺陷是缺少干燥装置.
(2)乙同学:实验过程中,往烧瓶中加入的浓氢氧化钠溶液一定要足量并充分加热,原因是NH4++OH-═NH3↑+H2O,使得NH4+全部转化为NH3,最终进入B装置被吸收.
【探究结论】
(3)称取27.0g硫酸铵化肥样品,用改进后的实验装置重新进行实验,测得实验后B装置增重6.8g.则该化肥含氮量为20.7%,由此可判断该化肥的品质.
17.我省要建成资源节约和生态保护型省份,下列措施或说法不符合这一理念的是( )
| A. | 做好空气质量预报工作,以便空气污染时及时采取防护措施 | |
| B. | 推广“绿色自由”计划,吸收空气中的CO2并利用廉价能源合成汽油 | |
| C. | 将工业废水“再生”处理,用于道路保洁、城市喷泉和洗车等 | |
| D. | 利用风能、生物能发电,强制实施火力发电用煤的脱硫处理 |
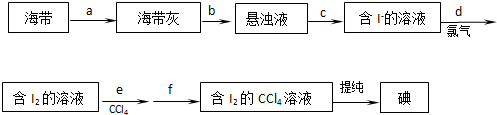
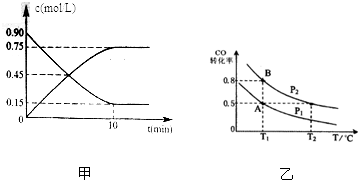
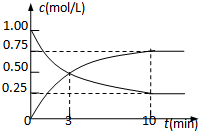 为实现“节能减排”和“低碳经济”的一项课题是如何将CO2转化为可利用资源.目前,工业上常用CO2来生产燃料甲醇.现进行如下实验:在体积为l L的密闭恒容容器中,充入l mol CO2和3mol H2,一定条件下发生反应:
为实现“节能减排”和“低碳经济”的一项课题是如何将CO2转化为可利用资源.目前,工业上常用CO2来生产燃料甲醇.现进行如下实验:在体积为l L的密闭恒容容器中,充入l mol CO2和3mol H2,一定条件下发生反应: