题目内容
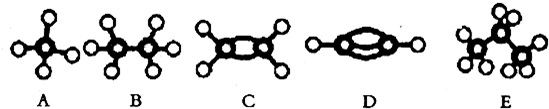
A~E是几种烃分子的球棍模型,据此回答下列问题:
(1)常温下含碳量最高的气态烃是 (填字母);
(2)能够发生加成反应的烃有 (填字母);
(3)一卤代物种类最多的是 (填字母);
(1)常温下含碳量最高的气态烃是
(2)能够发生加成反应的烃有
(3)一卤代物种类最多的是

考点:球棍模型与比例模型,饱和烃与不饱和烃
专题:有机化学基础
分析:有结构模型可知A为甲烷,B为乙烷,C为乙烯,D为乙炔,E为丙烷,根据物质的组成、结构和性质解答该题.
(1)常温下,分子中含有碳原子个数不大于4的烃为气态烃,根据其球棍模型判断,分子中含有碳氢原子个数比最大即为含碳量最高的.
(2)含有碳碳双键或三键或苯环的烃能发生加成反应.
(3)根据烃的球棍模型确定一卤代烃的同分异构体种类.
(1)常温下,分子中含有碳原子个数不大于4的烃为气态烃,根据其球棍模型判断,分子中含有碳氢原子个数比最大即为含碳量最高的.
(2)含有碳碳双键或三键或苯环的烃能发生加成反应.
(3)根据烃的球棍模型确定一卤代烃的同分异构体种类.
解答:
解:有结构模型可知A为甲烷,B为乙烷,C为乙烯,D为乙炔,E为丙烷,
(1)常温下,分子中含有碳原子个数不大于4的烃为气态烃,根据其球棍模型判断,分子中含有碳氢原子个数比最大即为含碳量最高的,所以含碳量最大的是乙炔.
故答案为:D.
(2)含有碳碳双键或三键或苯环的烃能发生加成反应,所以乙烯、乙炔、能发生加成反应,
故答案为:CD.
(3)甲烷、乙烷、乙烯、乙炔的一卤代物都只有1种,丙烷的一卤代物有2种,
故答案为:E.
(1)常温下,分子中含有碳原子个数不大于4的烃为气态烃,根据其球棍模型判断,分子中含有碳氢原子个数比最大即为含碳量最高的,所以含碳量最大的是乙炔.
故答案为:D.
(2)含有碳碳双键或三键或苯环的烃能发生加成反应,所以乙烯、乙炔、能发生加成反应,
故答案为:CD.
(3)甲烷、乙烷、乙烯、乙炔的一卤代物都只有1种,丙烷的一卤代物有2种,
故答案为:E.
点评:本题考查有机物的结构和性质,题目难度不大,注意把握有机物的结构特点,根据结构模型判断有机物的种类,为解答该题的关键.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
100mL某浓度的NaOH溶液中含有20g溶质.现欲配制1mol?L-1NaOH溶液,应取原溶液与蒸馏水的体积比约为( )
| A、4:1 | B、1:5 |
| C、1:4 | D、2:3 |
从硫化物中提取单质锑,经历以下两个过程:①2Sb2S3+3O2+6Fe
Sb4O6+6FeS ②Sb4O6+6C
4Sb+6CO↑关于反应①、②的说法不正确的是( )
| ||
| ||
| A、反应①中Sb元素被氧化 |
| B、反应②中Sb元素被还原 |
| C、标准状况下,每生成4 mol Sb时,消耗67.2LO2 |
| D、反应②说明高温下C的还原性比Sb强 |
纳米材料是指颗粒的三维线度中的任一维在1nm~100nm范围的材料.纳米技术所带动的技术革命及其对人类的影响,远远超过电子技术.下列关于纳米技术的叙述不正确的是( )
| A、将纳米材料分散到液体分散剂中可制得液溶胶 |
| B、用纳米级金属颗粒粉剂作为催化剂可加快化学反应速率 |
| C、将单质铜制成“纳米铜”时,具有非常强的化学活性,在空气中可以燃烧,说明“纳米铜”比铜片更易失电子 |
| D、银器能抑菌、杀菌,将纳米银粒子植入内衣织物中,有奇异的抑菌、杀菌效果 |
从物质的量浓度为1.0mol/L的NaOH溶液1L中取出100mL,下列关于100mL溶液的叙述中正确的是( )
| A、物质的量浓度为0.1 mol/L |
| B、含NaOH 0.01 mol |
| C、NaOH的物质的量浓度为1.0 mol/L |
| D、含NaOH 1 g |
某合作学习小组讨论辨析正确的是( )
①漂白粉和酸雨都是混合物;
②煤和石油都是可再生能源;
③蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质;
④不锈钢和目前流通的硬币都是合金;
⑤硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;
⑥豆浆和雾都是胶体.
①漂白粉和酸雨都是混合物;
②煤和石油都是可再生能源;
③蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质;
④不锈钢和目前流通的硬币都是合金;
⑤硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;
⑥豆浆和雾都是胶体.
| A、①②④⑤ | B、①②⑤⑥ |
| C、①③④⑥ | D、②③④⑤ |
下列起固氮作用的化学反应是( )
| A、N2与H2在一定条件下反应生成NH3 |
| B、NO与O2反应生成NO2 |
| C、由NH3制NH4HCO3和(NH4)2SO4 |
| D、NH3经催化氧化生成NO |
已知反应:①101kPa时,2C(s)+O2(g)═2CO(g)△H=-221kJ/mol;②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol.
下列结论正确的是( )
下列结论正确的是( )
| A、稀硫酸与稀NaOH溶液的中和热为57.3 kJ/mol |
| B、①的反应热为221 kJ/mol |
| C、稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ/mol |
| D、稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |