题目内容
下列过程方向的判断的说法中错误的是( )
| A、NH4NO3溶于水吸热,说明其溶于水不是自发过程 |
| B、等物质的量的同一种物质在气态时熵值最大,液态时次之,而固态时熵值最小 |
| C、不借助于外力能自发进行的反应过程,其体系的能量趋向于从高能状态转变为低能状态 |
| D、由能量判据和熵判据组合而成的复合判据,更适合于所有的反应过程 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A.吸热过程也可能是自发过程;
B.同种物质混乱度越大,熵越大;
C.物质的转化过程就是使物质趋向稳定的过程,物质的能量越低越稳定;
D.△H-T△S<0的过程属于自发过程.
B.同种物质混乱度越大,熵越大;
C.物质的转化过程就是使物质趋向稳定的过程,物质的能量越低越稳定;
D.△H-T△S<0的过程属于自发过程.
解答:
解:A.反应能否自发取决于焓变和熵变的复合判据,对于吸热反应,在一定温度下也能进行,NH4NO3溶于水是自发过程,故A错误;
B、同种物质混乱度越大,熵越大,则同一物质的固、液、气三种状态的熵值依次增大.故B正确;
C物质的转化过程就是使物质趋向稳定的过程,物质的能量越低越稳定,所以说不借助于外力能自发进行的过程,其体系的能量趋向于从高能状态转变为低能状态,故C正确;
D.反应能够自发进行的判断依据为:△H-T△S<0,所以反应能否自发进行与熵变和焓变都有关,故D正确;
故选A.
B、同种物质混乱度越大,熵越大,则同一物质的固、液、气三种状态的熵值依次增大.故B正确;
C物质的转化过程就是使物质趋向稳定的过程,物质的能量越低越稳定,所以说不借助于外力能自发进行的过程,其体系的能量趋向于从高能状态转变为低能状态,故C正确;
D.反应能够自发进行的判断依据为:△H-T△S<0,所以反应能否自发进行与熵变和焓变都有关,故D正确;
故选A.
点评:本题考查焓变和熵变与反应能否自发进行的关系,题目难度不大,注意反应能否自发进行,取决于自由能的大小,即:△H-T△S<0,与熵变和焓变都有关系.

练习册系列答案
相关题目
在强酸溶液中,下列各组离子能够大量共存的是( )
| A、Mg2+、Ca2+、HCO3-、Cl- |
| B、Na+、AlO2-、Cl-、SO42- |
| C、Cu2+、Fe3+、SO42-、MnO4- |
| D、K+、Fe2+、SO42-、NO3- |
在一个可以加热的密闭容器中,加入Na2O2和NaHCO3各0.5mol,将容器加热至400℃,待充分反应后排出气体,则容器中剩余的固体是( )
| A、Na2CO3 |
| B、Na2CO3和Na2O2 |
| C、NaOH |
| D、Na2CO3和NaOH |
关于如图装置的叙述,正确的是( )


| A、铝是负极,铝片上析出无色气体 |
| B、石墨是阳极,石墨棒上析出黄绿色气体 |
| C、溶液中两电极间产生白色沉淀 |
| D、溶液中先产生白色沉淀,最后沉淀溶解 |
化学与环境密切相关,下列说法正确的是( )
| A、CO2属于大气污染物 |
| B、酸雨是pH小于7的雨水 |
| C、CO2、NO2或SO2都会导致酸雨的形成 |
| D、大雾是一种胶体,能发生丁达尔效应 |
下列说法正确的是( )
| A、酸性氧化物一定是非金属氧化物,金属氧化物一定是碱性氧化物 |
| B、氢气中氢元素的化合价为0,所以氢分子中没有化学键 |
| C、离子键只存在于离子化合物中,而共价键可能存在于离子化合物或共价化合物中 |
| D、往饱和NaCl溶液中先通CO2至饱和,再往溶液中通NH3至饱和,可析出大量NaHCO3固体 |
临界状态指的是物质的气态和液态平衡共存时的一个边缘状态,在这种状态下,液体密度和饱和的蒸汽密度相同,因而他们的界面小时,这种状态只能在临界温度和临界压强下实现,可用临界点表示.二氧化硫的临界点为 157℃和78 atm,液态二氧化硫在25℃时的蒸汽压强为3.8 atm.试判断下列说法正确是( )
| A、二氧化硫的正常沸点在 25~157℃之间 |
| B、25℃贮有半满液态二氧化硫容器内的压力为5 atm |
| C、气态二氧化硫在150℃,80 atm时不能液化 |
| D、25℃和1 atm下二氧化硫是气体 |
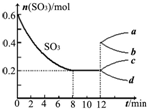 在一个2L的密闭容器中,发生反应2SO3(g)?2SO2(g)+O2(g)△H>0,其中SO3的变化如图所示:
在一个2L的密闭容器中,发生反应2SO3(g)?2SO2(g)+O2(g)△H>0,其中SO3的变化如图所示: