题目内容
16.某溶液中的阳离子有四种,分别是NH4+、Mg2+、Fe2+和Al3+,若向其中加入过量的NaOH溶液,微热并搅拌,再加入过量的盐酸,溶液中大量减少的金属离子是( )| A. | Fe2+ | B. | Mg2+ | C. | Al3+ | D. | NH4+ |
分析 加入过量的NaOH后,镁离子全部转化为Mg(OH)2沉淀.铝则转化成了偏铝酸根离子.氨转化为氨水,加热后生成氨气离开了溶液.铁离子全部转化为Fe(OH)2沉淀,被加热被氧化成Fe(OH)3,加入盐酸后氢氧化镁溶解生成氯化镁,氢氧化铁和盐酸反应生成氯化铁.
解答 解:依据题干信息分析判断可知,加入过量的NaOH后,镁离子全部转化为Mg(OH)2沉淀,铝则转化成了偏铝酸根离子,氨转化为氨水,加热后生成氨气离开了溶液,铁离子全部转化为Fe(OH)2沉淀,被加热被氧化成Fe(OH)3,加入盐酸后氢氧化镁溶解生成氯化镁,氢氧化铁和盐酸反应生成氯化铁;所以反应过程中金属离子大量减少的是Fe2+,故选A.
点评 本题考查离子之间的反应,明确阳离子与碱反应后的生成物的性质及生成物与酸的反应是解答本题的关键,注意亚铁离子易被氧化是学生解答中容易忽略的地方,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
6.一定温度下,在容积恒定的密闭容器中进行反应A(s)+2B(g)?C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是( )
①混合气体的密度不变
②容器内气体的压强不变
③混合气体的总物质的量不变
④B的物质的量浓度不变
⑤v正(C)=v逆(D)
⑥v正(B)=2v逆(C)
①混合气体的密度不变
②容器内气体的压强不变
③混合气体的总物质的量不变
④B的物质的量浓度不变
⑤v正(C)=v逆(D)
⑥v正(B)=2v逆(C)
| A. | ①④⑤⑥ | B. | ②③⑥ | C. | ②④⑤⑥ | D. | 只有④ |
4.下列溶液中,酸性最强的是( )
| A. | 0.01mol/L的盐酸 | B. | 0.01mol/L的醋酸溶液 | ||
| C. | c(H+)=10-3mol/L的溶液 | D. | c(OH-)=10-1mol/L溶液 |
11. 向容积固定为2L的密闭容器中充入9.6molNO和4.8molO2,发生如下反应:
向容积固定为2L的密闭容器中充入9.6molNO和4.8molO2,发生如下反应:
①2NO(g)+O2(g)?2NO2(g)△H<0
②2NO2(g)?N2O4(g)△H<0.
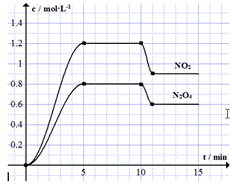
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T℃,10min时改变某反应条件,一段时间后再次平衡.下列说法正确的是( )
 向容积固定为2L的密闭容器中充入9.6molNO和4.8molO2,发生如下反应:
向容积固定为2L的密闭容器中充入9.6molNO和4.8molO2,发生如下反应:①2NO(g)+O2(g)?2NO2(g)△H<0
②2NO2(g)?N2O4(g)△H<0.
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T℃,10min时改变某反应条件,一段时间后再次平衡.下列说法正确的是( )
| A. | 前5min反应的平均速率v(NO)=0.24mol•(L•min)-1 | |
| B. | T℃时反应①的化学平衡常数K=0.36 | |
| C. | 10min时改变反应条件可能是降低温度 | |
| D. | 若起始时向该容器中充入1.6mol NO2和4.0mol N2O4,T℃达到平衡时,NO2的物质的量浓度与图中5~10min的不同 |
5. 某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.
某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.
(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭 真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
NH2COONH4(s)?2NH3(g)+CO2(g)
实验测得的不同温度下的平衡数据列于下表:
①可以判断该分解反应已经达到平衡的是BC.
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算 25.0℃时氨基甲酸铵的分解平衡常数:K=c2(NH3)•c(CO2)=($\frac{2}{3}$c总)2($\frac{1}{3}$c总)=$\frac{4}{27}$×(4.8×10-3)3=1.6×10-8.
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在 25.0℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量增加(填“增加”、“减少”或“不变”).
④氨基甲酸铵分解反应的焓变△H>0(填“>”、“=”或“<”),熵变△S>0(填“>”、“=”或“<”).
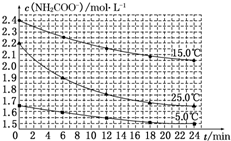
(2)已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定其水解反应速率,得到c(NH2COO-)随时间的变化趋势如图所示.
⑤计算 25.0℃时,0~6min 氨基甲酸铵水解反应的平均速率:0.05mol•L-1•min-1.
⑥根据图中信息,如何说明该水解反应速率随温度升高而增大:25.0℃时反应物的起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15.0℃时的大.
 某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.
某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭 真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
NH2COONH4(s)?2NH3(g)+CO2(g)
实验测得的不同温度下的平衡数据列于下表:
| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/mol•L-1 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 | 9.4×10-3 |
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算 25.0℃时氨基甲酸铵的分解平衡常数:K=c2(NH3)•c(CO2)=($\frac{2}{3}$c总)2($\frac{1}{3}$c总)=$\frac{4}{27}$×(4.8×10-3)3=1.6×10-8.
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在 25.0℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量增加(填“增加”、“减少”或“不变”).
④氨基甲酸铵分解反应的焓变△H>0(填“>”、“=”或“<”),熵变△S>0(填“>”、“=”或“<”).
(2)已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定其水解反应速率,得到c(NH2COO-)随时间的变化趋势如图所示.
⑤计算 25.0℃时,0~6min 氨基甲酸铵水解反应的平均速率:0.05mol•L-1•min-1.
⑥根据图中信息,如何说明该水解反应速率随温度升高而增大:25.0℃时反应物的起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15.0℃时的大.
10.欲除去下列物质中混入的少量杂质(括号内物质为杂质),不能达到目的是( )
| A. | 乙酸乙酯(乙酸):加饱和Na2CO3溶液,充分振荡静置后,分液 | |
| B. | 乙醇(水):加入新制生石灰,蒸馏 | |
| C. | 溴苯(溴):加入NaOH溶液,充分振荡静置后,分液 | |
| D. | 苯(苯酚):加浓溴水,静置后,过滤 |
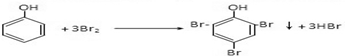 .
.