题目内容
10.玻璃棒是化学实验中常用的仪器,通常用于搅拌、引流等.下列有关实验过程中,不需要使用玻璃棒进行操作的是( )| A. | 用pH试纸测定Na2CO3溶液的pH | |
| B. | 从食盐水中提取NaCl | |
| C. | 用新制的FeSO4溶液和NaOH溶液制备Fe(OH)2 | |
| D. | 配制100ml 0.1000mol/L的NaCl溶液 |
分析 A.用pH试纸测定Na2CO3溶液的pH,可用玻璃棒蘸取溶液;
B.从食盐水中提取NaCl,用到过滤和蒸发操作;
C.无需使用玻璃棒;
D.配制一定物质的量浓度的溶液用玻璃棒搅拌和引流.
解答 解:A.用pH试纸溶液的pH,可用玻璃棒蘸取溶液,滴在玻璃片上的pH试纸上观察,故A正确;
B.从食盐水中提取NaCl,用到过滤和蒸发操作,分别用玻璃棒进行引流和搅拌,故B正确;
C.用新制的FeSO4溶液和NaOH溶液制备Fe(OH)2不需要使用玻璃棒,故C错误;
D.配制一定物质的量浓度的氯化钠溶液用玻璃棒搅拌和引流,故D正确.
故选C.
点评 本题考查化学实验基本操作,题目难度不大,注意常见化学基本操作以及实验的注意事项.

练习册系列答案
相关题目
15.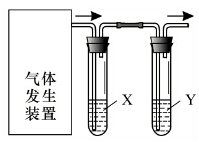 实验室用如图装置完成下表所列的四个实验,不能达到实验目的是( )
实验室用如图装置完成下表所列的四个实验,不能达到实验目的是( )
 实验室用如图装置完成下表所列的四个实验,不能达到实验目的是( )
实验室用如图装置完成下表所列的四个实验,不能达到实验目的是( ) | 选项 | 实验目的 | 试剂X | 试剂Y |
| A | 验证C2H5OH与浓H2SO4加热至170℃制得的乙烯的性质 | NaOH溶液 | Br2水 |
| B | 检验FeSO4受热分解产生的气体中由SO3和SO2 | BaCl2溶液 | 品红溶液 |
| C | 验证电石与饱和食盐水反应生成的乙炔的性质 | CuSO4溶液 | KMnO4溶液 |
| D | 验证氧化性:Cl2>Br2>I2 | NaBr溶液 | KI溶液 |
| A. | A | B. | B | C. | C | D. | D |
18.常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
请回答下列问题:
(1)不考虑其他组的结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸若pH=7,HA是强酸,若pH>7,则HA是弱酸.
(2)不考虑其他组的结果,单从乙组情况分析,c1是否一定等于0.2mol•L-1否?(填“是”或“否”).
混合溶液中c(A-)与c(Na+)离子浓度的大小关系是C(填序号).
A.前者大 B.后者大 C.一样大 D.无法判断
(3)从丙组结果分析,HA是弱酸(填“强”或“弱”).该混合溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+).
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=10-4mol•L-1.
| 实验编号 | HA物质的量浓度 (mol•L-1) | NaOH物质的量浓度 (mol•L-1) | 混合溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | C1 | 0.2 | pH=7 |
| 丙 | 0.1 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=10 |
(1)不考虑其他组的结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸若pH=7,HA是强酸,若pH>7,则HA是弱酸.
(2)不考虑其他组的结果,单从乙组情况分析,c1是否一定等于0.2mol•L-1否?(填“是”或“否”).
混合溶液中c(A-)与c(Na+)离子浓度的大小关系是C(填序号).
A.前者大 B.后者大 C.一样大 D.无法判断
(3)从丙组结果分析,HA是弱酸(填“强”或“弱”).该混合溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+).
(4)丁组实验所得混合溶液中由水电离出的c(OH-)=10-4mol•L-1.
15.实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH${\;}_{4}^{+}$+6HCHO═3H++6H2O+(CH2)6N4H+[滴定时,1mol(CH2)6N4H+与1mol H+相当],然后用NaOH标准溶液滴定反应生成的酸.某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ称取样品1.500g.
步骤Ⅱ将样品溶解后,完全转移到250mL容量瓶中,定容、充分摇匀.
步骤Ⅲ移取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次.
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数偏高(填“偏高”“偏低”或“无影响”).
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积无影响(填“偏大”“偏小”或“无影响”).
③滴定时边滴边摇动锥形瓶,眼睛应观察B.
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由无色变成浅红色.
(2)滴定结果如表所示:
若NaOH标准溶液的浓度为0.101 0mol•L-1,则该样品中氮的质量分数为18.85%.
步骤Ⅰ称取样品1.500g.
步骤Ⅱ将样品溶解后,完全转移到250mL容量瓶中,定容、充分摇匀.
步骤Ⅲ移取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次.
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数偏高(填“偏高”“偏低”或“无影响”).
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积无影响(填“偏大”“偏小”或“无影响”).
③滴定时边滴边摇动锥形瓶,眼睛应观察B.
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由无色变成浅红色.
(2)滴定结果如表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
2.下列反应中,盐酸既表现出酸性又表现出氧化性的是( )
| A. | 2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O | |
| B. | 2HCl$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑ | |
| C. | HCl+AgNO3═AgCl↓+HNO3 | |
| D. | Zn+2HCl═ZnCl2+H2↑ |
20.下列说法或表示方法正确的是( )
| A. | 甲烷的标准燃烧热为-890.3 kJ•molˉ1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•molˉ1 | |
| B. | 由C(石墨,s)=C(金刚石,s)△H=+1.9 kJ•molˉ1可知,金刚石比石墨稳定 | |
| C. | 在稀溶液中:H+(aq)+OHˉ(aq)=H2O(l)△H=-57.3 kJ•molˉ1,若将含1 mol CH3COOH与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJ | |
| D. | 一定条件下,某密闭容器中充入2 mol SO2(g)和1 mol O2(g),达到平衡后,放出Q kJ热量,则该条件下的热化学方程式为:2SO2(g)+O2(g)?2SO3(g )△H=-Q kJ•molˉ1 |