题目内容
中学化学中几种常见的转化关系如图所示(部分产物及反应条件为列出)已知A是金属单质,B为淡黄色粉末,DG在常温常压下为气态单质,J为红褐色沉淀.K俗称铁红
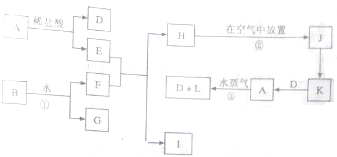
(1)写出下列物质的化学式:
A B D E K
(2)写出H→J过程的现象:
(3)写出下列反应的化学方程式
反应①
反应②
反应③ .

(1)写出下列物质的化学式:
A
(2)写出H→J过程的现象:
(3)写出下列反应的化学方程式
反应①
反应②
反应③
考点:无机物的推断
专题:
分析:A是金属单质,B为淡黄色粉末,能和水反应,生成气体单质G,则B为Na2O2,G为O2,F为NaOH,J为红褐色沉淀,则J为Fe(OH)3,K俗称铁红,则K为Fe2O3,根据各物质的转化关系,H为Fe(OH)2,则E为FeCl2,A为Fe,D为H2,I为NaCl,A与水蒸气反应生成H2和Fe3O4,则L为Fe3O4,据此答题.
解答:
解:A是金属单质,B为淡黄色粉末,能和水反应,生成气体单质G,则B为Na2O2,G为O2,F为NaOH,J为红褐色沉淀,则J为Fe(OH)3,K俗称铁红,则K为Fe2O3,根据各物质的转化关系,H为Fe(OH)2,则E为FeCl2,A为Fe,D为H2,I为NaCl,A与水蒸气反应生成H2和Fe3O4,则L为Fe3O4,
(1)根据上面的分析可知,A为Fe,B为Na2O2,D为H2,E为FeCl2,K为Fe2O3,
故答案为:Fe;Na2O2;H2;FeCl2;Fe2O3;
(2)H为Fe(OH)2,在空气中被氧化成氢氧化铁,这个过程的现象为白色沉淀变成灰绿色,最终变成红褐色,
故答案为:白色沉淀变成灰绿色,最终变成红褐色;
(3)反应①的化学方程式为2Na2O2+2H2O=4NaOH+O2↑,反应②的化学方程式为4Fe(OH)2+2H2O+O2=4Fe(OH)3,反应③的化学方程式为3Fe+4H2O
Fe3O4+4H2,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;4Fe(OH)2+2H2O+O2=4Fe(OH)3;3Fe+4H2O
Fe3O4+4H2;
(1)根据上面的分析可知,A为Fe,B为Na2O2,D为H2,E为FeCl2,K为Fe2O3,
故答案为:Fe;Na2O2;H2;FeCl2;Fe2O3;
(2)H为Fe(OH)2,在空气中被氧化成氢氧化铁,这个过程的现象为白色沉淀变成灰绿色,最终变成红褐色,
故答案为:白色沉淀变成灰绿色,最终变成红褐色;
(3)反应①的化学方程式为2Na2O2+2H2O=4NaOH+O2↑,反应②的化学方程式为4Fe(OH)2+2H2O+O2=4Fe(OH)3,反应③的化学方程式为3Fe+4H2O
| ||
故答案为:2Na2O2+2H2O=4NaOH+O2↑;4Fe(OH)2+2H2O+O2=4Fe(OH)3;3Fe+4H2O
| ||
点评:本题考查无机物的推断,题目难度不大,本题注意根据物质的性质、特征作为突破口进行推断,学习中注意牢固把握元素化合物的性质,不要忽视物质的用途.

练习册系列答案
相关题目
自来水可以用氯气消毒.某学生用这种自来水配制下列物质的溶液,不会产生明显药品变质的是( )
| A、NaOH |
| B、FeCl2 |
| C、NaHCO3 |
| D、FeCl3 |
下列各组离子在溶液中一定能够大量共存的是( )
| A、在含有大量AlO2-的溶液中:NO3-、Na+、Cl-、OH-. |
| B、在强碱溶液中:Na+、K+、CO32-、SO42- |
| C、在含有大量Fe3+的溶液中:NH4+、Na+、SCN-、Cl- |
| D、在含有大量Fe2+的溶液中:H+、Na+、Cl-、NO3- |
下列反应的离子方程式正确的是( )
| A、向溴水中加入NaOH溶液:Br2+2 OH-=BrO-+Br- |
| B、少量H2SO4滴入Ba(OH)2溶液中:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| C、过量NaHCO3溶液滴入NaHSO4溶液中:HCO3-+H+=H2O+CO2↑ |
| D、在漂白粉溶液中通入过量的CO2:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO |
下列石油的炼制和加工过程中,属于化学变化的是( )
| A、常压分馏 | B、减压分馏 |
| C、裂化 | D、裂解 |
在过量FeSO4溶液中滴入几滴NaClO溶液,并加入适量硫酸,溶液立即变为棕黄色.为检验上述反应中的还原产物,下列实验步骤中合理的组合是( )
①过滤,取滤液
②加入硝酸酸化的AgNO3溶液出现白色沉淀
③取一支试管,加入上述反应后的少许溶液
④再加入过量Ba(NO3)2溶液,出现白色沉淀
⑤再加入过量BaCl2,溶液,出现白色沉淀.
①过滤,取滤液
②加入硝酸酸化的AgNO3溶液出现白色沉淀
③取一支试管,加入上述反应后的少许溶液
④再加入过量Ba(NO3)2溶液,出现白色沉淀
⑤再加入过量BaCl2,溶液,出现白色沉淀.
| A、③⑤①② | B、③② |
| C、②③④⑤ | D、③④①② |
电解饱和食盐水时,在阴极区生成的物质是( )
| A、H2 、Cl2 |
| B、H2 、NaOH |
| C、H2 、H2O |
| D、Cl2、NaOH |
有一种纸质软电池,采用薄层纸片作为载体和传导体,一面附着锌,另一面附着二氧化锰.电池总反应为Zn+2MnO2+H2O=ZnO+2MnO(OH),关于此电池,下列说法中正确的是( )
| A、该电池Zn为负极,发生还原反应 |
| B、该电池的正极反应为MnO2+e-+H2O=MnO(OH)+OH- |
| C、放电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn |
| D、电池工作时OH-通过薄层纸片向附着二氧化锰的电极移动 |