题目内容
金属钙线是炼制优质钢材的脱氧脱磷剂,某钙线的主要成分为金属M和金属Ca,并含有3.5%(质量分数)CaO.
(1)Ca的原子结构示意图为 ,Ca(OH)2的碱性比Mg(OH)2 (填“强”或“弱”).
(2)Ca与非金属性最强的元素A形成化合物D,D的电子式为 .
(3)将钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色的M(OH)n,则金属M为 (填元素符号);检测Mn+ 最常用的试剂是 (填化学式).
(1)Ca的原子结构示意图为
(2)Ca与非金属性最强的元素A形成化合物D,D的电子式为
(3)将钙线试样溶于稀盐酸后,加入过量NaOH溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色的M(OH)n,则金属M为
考点:金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题,元素及其化合物
分析:(1)根据原子核外电子排布画出原子结构示意图;元素的金属性越强最高价氧化物对应的水化物的碱性越强;
(2)先判断最活泼的非金属元素,再确定该化合物的化学式,根据电子式书写规则写出电子式;根据晶体类型判断沸点高低;
(3)先判断Mn+离子是什么离子,再利用该离子的特殊反应检验;
(2)先判断最活泼的非金属元素,再确定该化合物的化学式,根据电子式书写规则写出电子式;根据晶体类型判断沸点高低;
(3)先判断Mn+离子是什么离子,再利用该离子的特殊反应检验;
解答:
解:(1)Ca是20号元素,元素的原子序数=其核外电子数=核内质子数,其核外电子排布是2,8,8,2,所以其原子结构示意图为 ,元素的金属性越强最高价氧化物对应的水化物的碱性越强,金属性Ca>Mg,所以Ca(OH)2的碱性比Mg(OH)2 强,故答案为
,元素的金属性越强最高价氧化物对应的水化物的碱性越强,金属性Ca>Mg,所以Ca(OH)2的碱性比Mg(OH)2 强,故答案为 ;强;
;强;
(2)、元素周期表中最活泼的非金属元素是F元素,与Ca形成化合物离子化合物D,所以D是CaF 2,其电子式为 ;故答案为:
;故答案为: ;
;
(3)根据题意知M(OH)n为请氧化铁,Mn+为Fe 3+,Fe 3+ 的检验方法是:向溶液中加入KSCN溶液后,溶液变成血红色就说明原溶液有Fe 3+,该反应的离子方程式为Fe+3SCN-=Fe(SCN)3,故答案为:Fe; KSCN(或NH4SCN).
 ,元素的金属性越强最高价氧化物对应的水化物的碱性越强,金属性Ca>Mg,所以Ca(OH)2的碱性比Mg(OH)2 强,故答案为
,元素的金属性越强最高价氧化物对应的水化物的碱性越强,金属性Ca>Mg,所以Ca(OH)2的碱性比Mg(OH)2 强,故答案为 ;强;
;强;(2)、元素周期表中最活泼的非金属元素是F元素,与Ca形成化合物离子化合物D,所以D是CaF 2,其电子式为
 ;故答案为:
;故答案为: ;
;(3)根据题意知M(OH)n为请氧化铁,Mn+为Fe 3+,Fe 3+ 的检验方法是:向溶液中加入KSCN溶液后,溶液变成血红色就说明原溶液有Fe 3+,该反应的离子方程式为Fe+3SCN-=Fe(SCN)3,故答案为:Fe; KSCN(或NH4SCN).
点评:通过本题,要掌握以下几点:
1、原子结构示意图与离子结构示意图的区别与联系;
2、离子化合物、共价化合物电子式的书写不同点;
3、三价铁离子的检验方法;
1、原子结构示意图与离子结构示意图的区别与联系;
2、离子化合物、共价化合物电子式的书写不同点;
3、三价铁离子的检验方法;

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
现有 W、X、Y、Z 四种物质,其中两种为单质,两种为化合物,且能发生反应:W+X→Y+Z,则Z不可能是( )
| A、Si |
| B、SO3 |
| C、Al2O3 |
| D、Fe3O4 |
下列关于摩尔质量的叙述正确的是( )
| A、氢气的摩尔质量是2 g |
| B、氢气的摩尔质量就是其相对分子质量 |
| C、氢的摩尔质量是2 g/mol |
| D、氢气的摩尔质量是2 g/mol |
鉴别下列各物质,只能用焰色反应的是( )
| A、NaCl和KCl |
| B、KCl和NaNO3 |
| C、NaCl和CuSO4 |
| D、NaCl和 K2CO3 |
打开盛头下列试剂瓶,有白雾现象的是( )
| A、浓硫酸 | B、浓硝酸 |
| C、稀硝酸 | D、浓盐酸 |
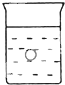 在一烧杯中盛有稀H2S04溶液.同时有一表面光滑的塑料小球悬浮于溶液中央,如图所示.向该烧杯里缓缓注入与稀H2SO4等密度的Ba(OH)2溶液至恰好完全反应.在此实验过程中
在一烧杯中盛有稀H2S04溶液.同时有一表面光滑的塑料小球悬浮于溶液中央,如图所示.向该烧杯里缓缓注入与稀H2SO4等密度的Ba(OH)2溶液至恰好完全反应.在此实验过程中 由徐光宪院士发起、院士学子同创的《分子共和国》科普读物最近出版了.全书形象生动地戏说了BF3、TiO2、CH3COOH、CO2、NO、二茂铁、NH3、HCN、H2S、O3、异戊二烯和萜等众多“分子共和国”中的明星.
由徐光宪院士发起、院士学子同创的《分子共和国》科普读物最近出版了.全书形象生动地戏说了BF3、TiO2、CH3COOH、CO2、NO、二茂铁、NH3、HCN、H2S、O3、异戊二烯和萜等众多“分子共和国”中的明星.