题目内容
在一定温度下,定容密闭容器中发生反应:H2(g)+I2(g)?2HI(g),下列能说明反应已达平衡状态的是( )
| A、容器内气体压强不再变化 |
| B、混合气体的密度恒定不变 |
| C、混合气体的颜色不再变化 |
| D、v正(H2)=v逆(HI) |
考点:化学平衡状态的判断
专题:
分析:根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A、容器内气体压强始终不变化,故A错误;
B、定容密闭容器中,混合气体的密度始终恒定不变,故B错误;
C、混合气体的颜色不再变化,说明碘蒸气的浓度不变,故C正确;
D、速率之比与计量数不成正比,故D错误;
故选:C.
B、定容密闭容器中,混合气体的密度始终恒定不变,故B错误;
C、混合气体的颜色不再变化,说明碘蒸气的浓度不变,故C正确;
D、速率之比与计量数不成正比,故D错误;
故选:C.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
下列说法或描述中,不符合实际的是( )
| A、医用药品应在低温、干燥的环境下密封保存 |
| B、反应中的某一物质的转化率α(B)增大,则该反应的平衡常数K一定增大 |
| C、向一堆篝火“鼓风”,有助于它继续燃烧下去 |
| D、微量的MnO2粉末可以使过氧化氢快速分解,而MnO2的质量在反应前后并没发生变化 |
下列离子在给定的条件下一定能大量共存的是( )
| A、加入Al粉放出H2的溶液中:Na+、K+、Fe3+、NO3- |
| B、c(Fe3+)=0.1mol/L的溶液中:NH4+、AlO2-、SO42-、HCO3- |
| C、水电离出的c(H+)=1×10-13mol/L的溶液中:Mg2+、K+、NO3-、Cl- |
| D、c(H+)=1×10-13mol/L的溶液中:K+、Cl-、AlO2-、CO3- |
下列有关化学键的叙述,正确的是( )
| A、离子化合物中不一定含有离子键 |
| B、单质分子中均不存在化学键 |
| C、由C元素形成的单质不一定是原子晶体 |
| D、含有共价键的化合物一定是共价化合物 |
下列说法正确的是( )
| A、摩尔是7个基本物理量之一 |
| B、18 g水在标准状况下的体积约为22.4 L |
| C、27 g Al约含有6.02×1023个铝原子 |
| D、配制0.1 mol/L的NaCl溶液需NaCl固体的质量为5.85 g |
短周期主族元素X、Y、Z、W,原子序数依次增大.X、Z同主族,X、Y、Z三种元素主族序数之和为15,Y原子最外层电子数等于X原子最外层电子数的一半.下列叙述正确的是( )
| A、非金属性:X<Z |
| B、原子半径:X<W<Z<Y |
| C、最高价氧化物对应水化物的酸性:W<Z |
| D、单质Y常温下能溶于浓硝酸 |
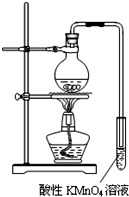 某学习小组探究溴乙烷的消去反应并验证产物.
某学习小组探究溴乙烷的消去反应并验证产物.