题目内容
20. 傅克反应是合成芳香族化合物的一种重要方法,有机物a和苯通过傅克反应合成b的过程表示如下(无机小分子产物略去):下列说法中不正确的是( )
傅克反应是合成芳香族化合物的一种重要方法,有机物a和苯通过傅克反应合成b的过程表示如下(无机小分子产物略去):下列说法中不正确的是( )| A. | 该反应是取代反应 | |
| B. | 若R为CH3时,a的电子式为 | |
| C. | 若R为C4H9时,b的结构可能有4种 | |
| D. | 若R为C4H20时,1 mol b最多可与5 mol H2加成 |
分析 A.由官能团的转化判断反应类型;
B.缺少Cl的核外最外层电子;
C.-C4H9有4种不同的结构;
D.R为C4H5时,含有2个碳碳双键和1个碳碳双键,且苯环也与氢气发生加成反应.
解答 解:A.烃基取代苯环的氢原子,为取代反应,故A正确;
B.缺少Cl的核外最外层电子,电子式错误,应为 ,故B错误;
,故B错误;
C.-C4H9有4种,分别为:①CH3-CH2-CH2-CH2-、②CH3-CH2-CH(CH3)-、③(CH3)2CH-CH2-、(④CH3)3C-,故C正确;
D.R为C4H5时,含有2个碳碳双键和1个碳碳双键,且苯环也与氢气发生加成反应,则1 mol b最多可与5 mol H2加成,故D正确.
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的官能团与性质的关系为解答的关键,侧重结构与性质的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)?2Z(g)△H<0,3min时达到平衡.此时Y的物质的量为0.10mol.反应过程中测定的数据如下表,下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前3min的平均速率v(Z)=2.0×10-5 mol/(L•min) | |
| B. | 其他条件不变,降低温度,反应达到新平衡前v(正)>v(逆) | |
| C. | 升高温度,该反应的平衡常数将增大 | |
| D. | 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大 |
15.化学与生活密切相关,下列有关说法错误的是( )
| A. | “地沟油”经过加工处理后,可以用来制肥皂和生物柴油 | |
| B. | 加热能杀死H7N9禽流感病毒是因为病毒的蛋白质受热变性 | |
| C. | 食品包装袋、食物保鲜膜等材料的主要成分是聚乙烯 | |
| D. | 纤维素作为营养物质,在人体内不断分解,最终生成水和二氧化碳排出体外 |
3.工业上用化学法除锅炉的水垢时,先向锅炉中注入饱和Na2CO3溶液浸泡,将水垢中的CaSO4转化为CaCO3,再用盐酸除去[已知:Ksp(CaCO3)=1×1010,Ksp(CaSO4)=9×10-6].下列说法错误的是( )
| A. | 温度升高,Na2CO3溶液的Ksp和c(OH-)均会增大 | |
| B. | 沉淀转化的离子方程式为CO32-(aq)+CaSO4(s)?CaCO3(s)+SO42-(aq) | |
| C. | 该条件下,CaCO3的溶解度约为1×10-3g | |
| D. | CaCO3和CaSO4共存的悬浊液中,$\frac{c(S{{O}_{4}}^{2-})}{c(C{{O}_{3}}^{2-})}$=9×104 |
10.下列有关物质的性质与用途具有对应关系的是( )
| A. | 漂白粉在空气中不稳定,可用于漂白纸张 | |
| B. | 氨气具有还原性,可用作制冷剂 | |
| C. | Na2O2呈浅黄色,可用作潜水艇中的供氧剂 | |
| D. | 明矾水解形成Al(OH)3胶体,可用作水处理中的净水剂 |
7.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.1 mol甲烷含有的电子数为NA | |
| B. | 1L0.1mol/LNa2CO3溶液中含有的CO32-数目为0.1NA | |
| C. | 1mol-OH (羟基)与l molOH-均含有10个NAe- | |
| D. | 标准状况下,2.24LCO和CO2混合气体中含有的氧原子数为0.15NA |
8.下列关于物质的用途或说法不正确的是( )
| A. | 氧化铝熔点很高,可用作耐火材料 | |
| B. | 铝热反应原理是炼铁最常用的反应原理 | |
| C. | 过氧化钠可以用作呼吸面具中的供氧剂 | |
| D. | 青铜是我国使用最早的合金 |
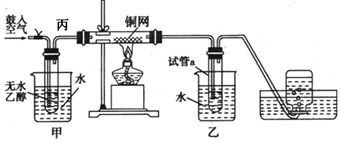
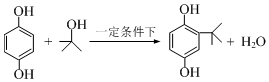
 2-叔丁基对苯二酚是一种重要的食品抗氧剂,现以对苯二酚、叔丁醇为原料,一定条件下经Freidel-Crafts 烷基化反应合成.原理如下:
2-叔丁基对苯二酚是一种重要的食品抗氧剂,现以对苯二酚、叔丁醇为原料,一定条件下经Freidel-Crafts 烷基化反应合成.原理如下: