题目内容
NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,22.4L以任意比混和的甲烷和氢气的混合物,所含的分子数为NA个 |
| B、标准状况下,32g氧气所含的原子数目为NA |
| C、在25℃,压强为1.01×105Pa时,22.4L水所含的分子数为NA个 |
| D、1 mol/L的盐酸中含NA个HCl分子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、根据标况下的气体摩尔体积进行计算;
B、根据氧气的质量计算出物质的量,再计算出含有氧原子的物质的量及数目;
C、不是标准状况下,水不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
D、盐酸的体积没有告诉,无法计算氯化氢的分子数.
B、根据氧气的质量计算出物质的量,再计算出含有氧原子的物质的量及数目;
C、不是标准状况下,水不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
D、盐酸的体积没有告诉,无法计算氯化氢的分子数.
解答:
解:A、标况下气体摩尔体积为22.4L/mol,22.4L甲烷和气体的物质的量为1mol,所含的分子数为NA个,故A正确;
B、32g氧气的物质的量为1mol,含有2mol氧原子,含的原子数目为2NA,故B错误;
C、不是标况下,水也不是气体,题中条件无法计算水的质量,无法计算22.4L水的物质的量及分子数,故C错误;
D、没有告诉1 mol/L的盐酸的体积,无法计算氯化氢的物质的量,故D错误;
故选A.
B、32g氧气的物质的量为1mol,含有2mol氧原子,含的原子数目为2NA,故B错误;
C、不是标况下,水也不是气体,题中条件无法计算水的质量,无法计算22.4L水的物质的量及分子数,故C错误;
D、没有告诉1 mol/L的盐酸的体积,无法计算氯化氢的物质的量,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意标况下的条件要求及物质的状态,要求学生掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.

练习册系列答案
相关题目
菜谱中记载:河虾不宜与西红杮同食,主要原因是河虾中含有+5价砷,西红杮中含有比较多的维生素C,两者同食会产生有毒的+3价砷,下列说法中正确的是( )
| A、中毒的过程中,+5价砷体现出一定的还原性 |
| B、中毒的过程中,维生素C作氧化剂 |
| C、因为河虾中含有砷元素,所以不能食用 |
| D、+3价砷具有还原性 |
下列化学用语正确的是( )
| A、乙烯的结构简式为:CH2CH2 |
| B、苯的分子式为:C6H6 |
| C、羟基的电子式为:-O-H |
D、甲烷分子的比例模型: |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、1 mol/L的硫酸溶液中含有的H+数约为2NA |
| B、常温常压下,18 g水中含有的水分子数为NA |
| C、标准状况下,22.4 L氯化氢所含的原子数为NA |
| D、24 g O2分子和24 g O3分子所含的氧原子数目相等 |
已知:Ni+CuSO4=NiSO4+Cu Cu+2AgNO3=Cu(NO3)2+2Ag 则下列判断正确的是( )
| A、还原性:Ni>Cu>Ag |
| B、氧化性:Ni2+>Cu2+>Ag+ |
| C、还原性:Ni<Cu<Ag |
| D、氧化性:Ni2+<Cu2+<Ag+ |

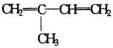 与 CH2=CH2 发生加成反应产物的结构简式(或键线式)
与 CH2=CH2 发生加成反应产物的结构简式(或键线式)