题目内容
在10℃和2×105Pa的条件下,反应aA(g)?dD(g)+eE(g)建立平衡后再逐步增大体系的压强(温度不变).下表列出了不同压强下反应建立平衡时物质D的浓度:
根据表中数据回答:
(1)压强从2×105Pa增加到5×105Pa时,平衡向 反应方向移动(填“正”、“逆”),理由是 .
(2)压强从5×105Pa增加到1×106Pa时,平衡向 反应方向移动(填“正”、“逆”),理由是 ;可能原因是 .
| 压强(Pa) | 2×105 | 5×105 | 1×106 |
| D的浓度(mol/L) | 0.085 | 0.20 | 0.44 |
(1)压强从2×105Pa增加到5×105Pa时,平衡向
(2)压强从5×105Pa增加到1×106Pa时,平衡向
考点:化学平衡的影响因素
专题:化学平衡专题
分析:(1)压强从2×105Pa增加到5×105 Pa时,D的浓度应变化应该为0.2125mol/L,而图表中变化为0.20mol/L<0.2125mol/L,说明平衡逆向进行;
(2)5×106 Pa 增加到1×106 Pa时,D的浓度应变化为0.20mol/L的2倍即0.4mol/L,而图表中D的浓度为0.44mol/L,说明平衡正向进行.
(2)5×106 Pa 增加到1×106 Pa时,D的浓度应变化为0.20mol/L的2倍即0.4mol/L,而图表中D的浓度为0.44mol/L,说明平衡正向进行.
解答:
解:(1)压强从2×105Pa增加到5×105 Pa时,D的浓度应变化为0.085mol/L的2.5倍即为0.2125mol/L,而图表中变化为0.20mol/L<0.2125mol/L,说明平衡逆向进行,
故答案为:逆;加压时生成物D浓度增大的倍数小于压强增大的倍数;
(2)压强从5×106 Pa 增加到1×106 Pa时,D的浓度应变化为0.20mol/L的2倍即0.4mol/L,而图表中D的浓度为0.44mol/L,说明平衡正向进行,其原因是:由于加压后E物质液化使平衡正移,故答案为:正;压强增大2.0倍,而浓度却增大2.2倍,说明反应向正反应方向进行;由于加压后E物质液化使平衡正移.
故答案为:逆;加压时生成物D浓度增大的倍数小于压强增大的倍数;
(2)压强从5×106 Pa 增加到1×106 Pa时,D的浓度应变化为0.20mol/L的2倍即0.4mol/L,而图表中D的浓度为0.44mol/L,说明平衡正向进行,其原因是:由于加压后E物质液化使平衡正移,故答案为:正;压强增大2.0倍,而浓度却增大2.2倍,说明反应向正反应方向进行;由于加压后E物质液化使平衡正移.
点评:本题考查了化学平衡状态的影响因素,关键是分析题中表格的数据,得出正确结论,充分考查了学生的分析、理解能力,是一道不错的题目,本题难度中等.

练习册系列答案
相关题目
2011年11月1日我国天宫一号与神舟八号成功对接,“嫦娥”探月工程也正在如火如荼进行中.科学家预测,月球的土壤中有数百万吨32He,每百吨32He核聚变释放出的能量相当于目前人类一年消耗的能量.在地球上,氦元素主要以42He的形式存在.下列说法正确的是( )
| A、42He原子核内含有4个质子 |
| B、32He和42He互为同位素 |
| C、32He原子核内含有3个中子 |
| D、32He和42He互为同素异形体 |
下列实验操作正确的是( )
| A、倾倒液体时试剂瓶上的标签握在手心 |
| B、称量药品时用手取砝码 |
| C、稀释浓硫酸时将水倒入浓硫酸中 |
| D、用燃着的酒精灯去点燃另一酒精灯 |
一定条件下,体积为10L的密闭容器中,2mol X和1mol Y进行反应:2X(g)+Y(g)?Z(g)△H<0,经20s达到平衡,生成0.5mol Z.下列说法正确的是( )
| A、该反应平衡常数的值为1 |
| B、将容器体积变为20L,Z的平衡浓度减小为0.025mol/L |
| C、以X浓度变化表示的反应速率为0.005mol/(L?s) |
| D、当X、Y、Z的浓度相等时,证明反应达到平衡状态 |
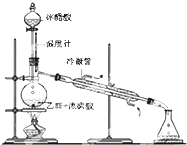 有机化学知识在生活中应用广泛.
有机化学知识在生活中应用广泛.

 铜锌原电池装置如图.请回答:
铜锌原电池装置如图.请回答: