题目内容
10.乙醇分子中不同的化学键如图所示,下列不同反应中键的断裂不正确的是( )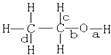
| A. | 和乙酸发生酯化反应键a断裂 | |
| B. | 和浓硫酸共热至170℃时键b和d断裂 | |
| C. | 在铜催化和加热条件下和氧气反应键a、c断裂 | |
| D. | 和氢溴酸反应键a断裂 |
分析 A.酯化反应时醇脱H;
B.发生消去反应生成生成乙烯;
C.发生催化氧化生成乙醛;
D.与HBr发生取代反应,-OH被-Br取代.
解答 解:A.酯化反应时醇脱H,O-H键断裂,即键a断裂,故A正确;
B.发生消去反应生成生成乙烯,则键b和d断裂,故B正确;
C.发生催化氧化生成乙醛,则键a、c断裂,故C正确;
D.与HBr发生取代反应,-OH被-Br取代,则键b断裂,故D错误;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、化学键的断裂为解答的关键,侧重分析与应用能力的考查,注意醇的性质及应用,题目难度不大.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
19.下列说法中不正确的是( )
①将硫酸钡放入水中不能导电,所以硫酸钡是非电解质
②氨溶于水得到的溶液氨水能导电,所以氨是电解质
③固态共价化合物可以导电
④固态的离子化合物不导电,熔融态的离子化合物也不导电
⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强.
①将硫酸钡放入水中不能导电,所以硫酸钡是非电解质
②氨溶于水得到的溶液氨水能导电,所以氨是电解质
③固态共价化合物可以导电
④固态的离子化合物不导电,熔融态的离子化合物也不导电
⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强.
| A. | ①④ | B. | ①④⑤ | C. | ①②③④ | D. | ①②③④⑤ |
1.在一定温度下,反应$\frac{1}{2}$H2(g)$+\frac{1}{2}$X2(g)?HX(g)的平衡常数为9.若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于( )
| A. | 10% | B. | 18% | C. | 20% | D. | 40% |
18.下列物质不属于有机物的是( )
| A. | C2H6 | B. | C12H22O11 | C. | C6H12O6 | D. | CaCO3 |
5.裂解水制氢气的过程如图所示.下列说法不正确的是( )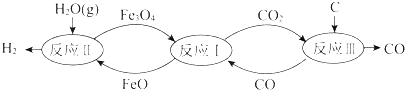

| A. | 反应Ⅰ的化学方程式是Fe3O4+CO?3FeO+CO2 | |
| B. | 反应Ⅱ的化学方程式是3FeO+H2O(g)?Fe3O4+H2 | |
| C. | 总反应的化学方程式是C+2H2O(g)?CO2+2H2 | |
| D. | 铁的氧化物是裂解水的催化剂 |
2.下列各项中的两个量,其比值一定为2:l的是( )
| A. | 在反应2 H2S+SO2→3 S+2 H2O中被氧化与被还原的硫原子的质量 | |
| B. | 相同温度下,0.2 mol•L-1 CH3COOH溶液与0.1 mol•L-1 CH3COOH溶液中的c(H+) | |
| C. | 在密闭容器中,N2+3H2?2NH3达平衡时的c(NH3)与c(N2) | |
| D. | Na2CO3晶体中Na+与CO32-离子个数比 |
19. 水杨酸甲酯对多种细菌的繁殖和黏附有抑制作用,也是安全、有效的植物生长调节剂.实验室制备水杨酸甲酯装置示意图和有关数据如下:
水杨酸甲酯对多种细菌的繁殖和黏附有抑制作用,也是安全、有效的植物生长调节剂.实验室制备水杨酸甲酯装置示意图和有关数据如下:
 +CH3OH$\stackrel{H+}{?}$
+CH3OH$\stackrel{H+}{?}$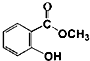 +H2O
+H2O
实验步骤:
①在干燥的三颈烧瓶中入7.0g水杨酸、30mL(0.64moL)甲醇、3mL浓H2SO4和2~3片碎瓷片,在85~95℃下加热回流(如图甲);
②1.5h后将回流装置改为蒸馏装置,水浴加热(如图乙);
③余下的反应液冷却至室温,依次用水、碳酸钠溶液和水洗涤,后再分离(如图丙);
④分出的产物加入少量无水CaCl2固体,静置片刻后过滤,
⑤对滤液蒸馏纯化,收集221~224℃馏分,得水杨酸甲酯6.1g.
⑥其它量不变,改用2mL浓H2SO4重复上述操作,得水杨酸甲酯5.5g.
回答下列问题:
(1)甲中所用三颈烧瓶应选用A
A.100mL B.150mL C.250mL D.500mL
(2)整个实验两次用到蒸馏装置,第一次用蒸馏装置的目的是:甲醇有毒,用于回收甲醇.
(3)步骤③中所用到的玻璃仪器的名称是分液漏斗、锥形瓶;
(4)本实验甲醇要过量,其目的是提高水杨酸的转化率,
(5)步骤③要进行两次水洗,如果没有进行第二次水洗,可能的后果是残留的碳酸钠与CaCl2反应生成沉淀堵塞分液漏斗,并在蒸馏时会促进水杨酸甲酯的水解.
(6)浓H2SO4的用量为3mL时,水杨酸甲酯的产率是79.2%,
(7)该实验中,浓硫酸主要表现了催化、吸水性质.
 水杨酸甲酯对多种细菌的繁殖和黏附有抑制作用,也是安全、有效的植物生长调节剂.实验室制备水杨酸甲酯装置示意图和有关数据如下:
水杨酸甲酯对多种细菌的繁殖和黏附有抑制作用,也是安全、有效的植物生长调节剂.实验室制备水杨酸甲酯装置示意图和有关数据如下:| 相对分子 质量 | 沸点/℃: | 在水中的溶解性 | |
| 甲醇 | 32 | 64.7 | 与水以任何比例相溶 |
| 水杨酸 | 138 | 211 | 0.22g/100ml |
| 水杨酸甲酯 | 152 | 222 | 0.07g/100ml |
 +CH3OH$\stackrel{H+}{?}$
+CH3OH$\stackrel{H+}{?}$ +H2O
+H2O实验步骤:
①在干燥的三颈烧瓶中入7.0g水杨酸、30mL(0.64moL)甲醇、3mL浓H2SO4和2~3片碎瓷片,在85~95℃下加热回流(如图甲);
②1.5h后将回流装置改为蒸馏装置,水浴加热(如图乙);
③余下的反应液冷却至室温,依次用水、碳酸钠溶液和水洗涤,后再分离(如图丙);
④分出的产物加入少量无水CaCl2固体,静置片刻后过滤,
⑤对滤液蒸馏纯化,收集221~224℃馏分,得水杨酸甲酯6.1g.
⑥其它量不变,改用2mL浓H2SO4重复上述操作,得水杨酸甲酯5.5g.
回答下列问题:
(1)甲中所用三颈烧瓶应选用A
A.100mL B.150mL C.250mL D.500mL
(2)整个实验两次用到蒸馏装置,第一次用蒸馏装置的目的是:甲醇有毒,用于回收甲醇.
(3)步骤③中所用到的玻璃仪器的名称是分液漏斗、锥形瓶;
(4)本实验甲醇要过量,其目的是提高水杨酸的转化率,
(5)步骤③要进行两次水洗,如果没有进行第二次水洗,可能的后果是残留的碳酸钠与CaCl2反应生成沉淀堵塞分液漏斗,并在蒸馏时会促进水杨酸甲酯的水解.
(6)浓H2SO4的用量为3mL时,水杨酸甲酯的产率是79.2%,
(7)该实验中,浓硫酸主要表现了催化、吸水性质.
20.如图是元素周期表的一部分.X、Y、Z、W均为短周期元素,Z元素原子最外层电子数是电子层数的2倍.下列说法不正确的是( )
| X | Y | ||
| Z | W |
| A. | W 的最高价氧化物的水化物酸性比Z的强 | |
| B. | 原子半径:Z>W,离子半径:Z<W | |
| C. | Y的气态氢化物可与W的气态氢化物反应生成一种离子化合物 | |
| D. | X元素形成的化合物种类最多 |