题目内容
15.关于钠的叙述中,不正确的是( )| A. | 金属钠与水反应庄成氢气,但是实验室中不能用金属钠与水反应制备氢气 | |
| B. | 金属钠放在石棉网上加热时,先熔化成银白色小球,然后剧烈燃烧,发出黄色火焰 | |
| C. | 金属钠在空气中放置会生成氧化钠,在空气中燃烧则会生成过氧化钠 | |
| D. | 金属钠与氧气反应的产物取决于氧气的用量 |
分析 钠性质活泼,易与水、氧气反应,常温下,钠与氧气反应生成过氧化钠,钠燃烧生成过氧化钠,钠的熔点较大,与水反应时放出的热量可使钠熔化,以此解答该题.
解答 解:A.实验室一般用锌和盐酸反应制备氢气,由于钠的价格较高,不能用钠和水反应制备氢气,故A正确;
B.钠的熔点较大,加热易熔化,加热条件下钠和氧气反应生成过氧化钠,火焰呈黄色,故B正确;
C.常温下钠易和氧气反应生成氧化钠,在点燃条件下反应生成过氧化钠,故C正确;
D.如在常温下,钠与氧气反应生成氧化钠,与氧气的量无关,故D错误.
故选D.
点评 本题考查钠的性质,为高频考点,侧重考查学生的双基知识,题目难度不大,注意把握钠与水、氧气反应的特点.

练习册系列答案
相关题目
5.下列说法正确的是( )
| A. | 化学实验产生的废液应及时倒入下水道 | |
| B. | 实验室的废酸或废碱可用中和法来处理 | |
| C. | 实验用剩的钾、钠等金属要即时扔进废液缸 | |
| D. | 如果酸洒在实验桌上,立即用氢氧化钠溶液中和 |
3.火法炼铜首先要焙烧黄铜矿,反应为:2CuFeS2+O2=Cu2S+2FeS+SO2则下列说法正确的是( )
| A. | CuFeS 2 仅作还原剂,硫元素被氧化 | |
| B. | 每生成1mol Cu2 S,有4 mol硫被氧化 | |
| C. | SO 2 只是氧化产物,FeS只是还原产物 | |
| D. | 每转移1.2 mol电子,有0.2mol硫被氧化 |
10.下列分子或离子在指定的分散系中能大量共存的一组是( )
| A. | 水溶液中:K+、Ca2+、C1-、NO${\;}_{3}^{-}$ | |
| B. | 空气:CH4、CO2、SO2、NO | |
| C. | 氢氧化铁胶体:H+、K+、S2-、Br- | |
| D. | 高锰酸钾溶液:H+、Na+、SO${\;}_{4}^{2-}$、I- |
1.下列说法正确的是( )
| A. | 燃料电池的电极包含活性物质,参与电极反应 | |
| B. | 氢氧燃料电池工作时发出蓝色火焰 | |
| C. | 铁在干燥的空气中不易生锈,在潮湿的空气中易生锈,主要是因发生电化腐蚀 | |
| D. | 温度一定时,催化剂不仅可以加快化学反应速率,而且可以改变反应物的转化率 |

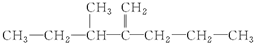 ,此烃名称为3-甲基-2-丙基-1-戊烯
,此烃名称为3-甲基-2-丙基-1-戊烯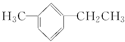 ,可命名为1-甲基-3-乙基苯(或3-甲基乙苯或间甲基乙苯);.
,可命名为1-甲基-3-乙基苯(或3-甲基乙苯或间甲基乙苯);.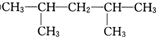
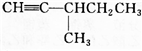 .
.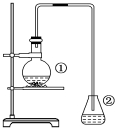 为探究苯与溴的取代反应,甲用如图装置进行如下实验:将一定量的苯和溴放在烧瓶中,同时加入少量铁屑,3~5min后发现滴有AgNO3的锥形瓶中有浅黄色的沉淀生成,即证明苯与溴发生了取代反应.
为探究苯与溴的取代反应,甲用如图装置进行如下实验:将一定量的苯和溴放在烧瓶中,同时加入少量铁屑,3~5min后发现滴有AgNO3的锥形瓶中有浅黄色的沉淀生成,即证明苯与溴发生了取代反应. ②中离子方程式为Br-+Ag+═AgBr↓.
②中离子方程式为Br-+Ag+═AgBr↓.