题目内容
3.短周期元素X、Y、Z、W、Q的原子序数依次增大,X与Q同主族,X的最外层电子数是次外层电子数的2倍,W的最外层电子数等于其电子层数,Y与Z的核外电子数之和等于X与Q的核外电子数之和,下列说法正确的是( )| A. | Z、W、Q、X、Y原子半径依次减小 | |
| B. | W最高价氧化物对应水化物一定能溶于Z最高价氧化物对应水化物的溶液中 | |
| C. | Y与Q形成化合物在常温下一定为气态 | |
| D. | Z、Q元素的单质都可以将X元素的单质从其氧化物中置换出来 |
分析 X的最外层电子数是次外层电子数的2倍,应为C元素,X与Q同主族,则Q为Si元素,W的最外层电子数等于其电子层数,由原子序数关系可知为Al元素,Y与Z的核外电子数之和等于X与Q的核外电子数之和,则Y与Z的核外电子数之和为6+14=20,Y可能为O、F元素,Z可能为Mg、Na等元素,结合对应单质、化合物的性质以及元素周期率解答该题.
解答 解:由以上分析可知X为C、Y可能为O、F元素,Z可能为Mg、Na等元素,W为Al元素、Q为Si元素,
A.同周期元素从左到右原子半径逐渐减小,同主族从上到下逐渐增大,则Z、W、Q、X、Y原子半径依次减小,故A正确;
B.如Z为Mg,则氢氧化铝与氢氧化镁不反应,故B错误;
C.Y与Q形成化合物如为二氧化硅,则为固体,故C错误;
D.Si和二氧化碳不反应,故D错误.
故选A.
点评 本题考查了元素的位置、结构和性质,为高考常见题型和高频考点,侧重考查学生的分析能力,正确推断元素是解本题关键,结合元素周期律来分析解答,难度中等.

练习册系列答案
相关题目
13.下列现象不适宜用勒夏特列原理解释的是( )
| A. | 工业上用Na2CO3溶液浸泡水垢 | B. | 夏天的食物更易腐败变质 | ||
| C. | 将氨水保存在温度较低处 | D. | 热的纯碱溶液去除油污效果更好 |
15.常温下,下列物质的溶液中粒子浓度关系不正确的是( )
| A. | pH=1的KHSO4溶液:c(H+)=c(SO42-)+c(OH-) | |
| B. | CH3COONa和BaCl2混合溶液:c(Na+)+c(Ba2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) | |
| C. | 三种相同浓度的铵盐溶液中c(NH4+)从大到小的顺序:NH4HSO4、NH4Cl、NH4HCO3 | |
| D. | 已知AgCl、AgBr、AgI溶度积常数依次为1.6×l0-10、7.7×10-13、8.7×10-17,则对应饱和溶液中c(X-)从大到小的顺序为:Cl-、Br-、I- |
11.如图是部分短周期元素原子半径与原子序数的关系图.则下列说法正确的是( )

| A. | Z、M的单质均不能与冷水反应 | |
| B. | 最高价氧化物对应水化物的酸性:R<N | |
| C. | 气态氢化物的热稳定性:Y<N<R | |
| D. | 简单离子半径:M<Z<Y<X |
18.下列说法不正确的是( )
| A. | 生铁、不锈钢和黄铜都属于合金 | |
| B. | 淀粉、油脂和蛋白质都属于天然高分子化合物 | |
| C. | 水泥、玻璃和陶瓷都属于无机非金属材料 | |
| D. | 天然气、液化石油气和汽油的主要成分都属于烃类 |
14.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将某有机物与溴的四氯化碳溶液混合 | 溶液褪色 | 该有机物中必定含有碳碳双键 |
| B | 向亚硫酸钠溶液中滴加硝酸钡和稀硝酸 | 产生白色沉淀 | 亚硫酸钠溶液已变质 |
| C | 向酸性高锰酸钾溶液中滴加双氧水 | 紫色褪去,产生气泡 | H2O2具有还原性 |
| D | 向油脂皂化反应后的溶液中滴入酚酞 | 溶液不变红 | 油脂已经完全皂化 |
| A. | A | B. | B | C. | C | D. | D |
10.下列各化合物中,阳离子半径最大而阴离子半径最小的是( )
| A. | KF | B. | AlCl3 | C. | NaI | D. | MgBr2 |
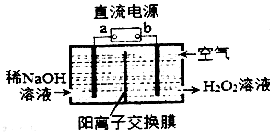 H2O2是一种常用绿色氧化剂,工业上利用电解法制备H2O2的装置如图所示:
H2O2是一种常用绿色氧化剂,工业上利用电解法制备H2O2的装置如图所示: 、K+
、K+ 、NO
、NO
 、ClO-
、ClO- )=0.1 mol·L-1的溶液中:Na+、Cl-、H+、Ca2+
)=0.1 mol·L-1的溶液中:Na+、Cl-、H+、Ca2+