��Ŀ����
10��t��ʱ����2mol����A��1mol����B�����ݻ�Ϊ2L�ĺ����ܱ������У��������·�Ӧ��2A��g��+B��g��?xC��g����2minʱ��ѧ��Ӧ�ﵽ�ȣ��¶���Ϊt�棩����ʱB���� 0.6mol�������C��Ũ��Ϊ0.6mol•L-1����ش��������⣺
��1���жϸ÷�Ӧ�ﵽ�ȵı�־��bd
a�������е�ѹǿ���ֲ���
b��A������������B����������֮��Ϊ2��1
c�������ڻ��������ܶȱ��ֲ���
d��A�İٷֺ������ֲ���
e��B��C�����ʵ���Ũ��֮��Ϊ1��x
��2��x=3���ӷ�Ӧ��ʼ���ﵽ��ʱ����B��ʾ�÷�Ӧ��ƽ����Ӧ����V��B��=0.1mol•L-1•min-1��
��3���������¶Ȳ��䣬�������������������Ӧ���ʼ�С�����������С�����䡱��
��4����ѧ��Ӧ�ﵽ��ʱ��A��ת����Ϊ40%��
���� 2minʱ��ѧ��Ӧ�ﵽ�ȣ��¶���Ϊt�棩����ʱB���� 0.6mol��ת����BΪ$\frac{1mol-0.6mol}{2L}$=0.2mol/L�������C��Ũ��Ϊ0.6mol•L-1����$\frac{1}{x}=\frac{0.2}{0.6}$�����x=3����
2A��g��+B��g��?3C��g��
��ʼ 2 1 0
ת�� 0.8 0.4 1.2
ƽ�� 1.2 0.6 1.2
��1�����ƽ����������ȡ��������������������жϣ�
��2�����v=$\frac{��c}{��t}$���㣻
��3�������¶Ȳ��䣬�������������ѹǿ��С��
��4�����ת����=$\frac{ת������}{��ʼ����}$��100%���㣮
��� �⣺2minʱ��ѧ��Ӧ�ﵽ�ȣ��¶���Ϊt�棩����ʱB���� 0.6mol��ת����BΪ$\frac{1mol-0.6mol}{2L}$=0.2mol/L�������C��Ũ��Ϊ0.6mol•L-1����$\frac{1}{x}=\frac{0.2}{0.6}$�����x=3����
2A��g��+B��g��?3C��g��
��ʼ 2 1 0
ת�� 0.8 0.4 1.2
ƽ�� 1.2 0.6 1.2
��1��a���÷�ӦΪ�����������ķ�Ӧ���������е�ѹǿ���ֲ��䣬�����ж�ƽ�⣬�ʲ�ѡ��
b��A������������B����������֮��Ϊ2��1��Ϊ��ͬ���ʵ����淴Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ��ﵽƽ��״̬����ѡ��
c��������������䣬�������ڻ��������ܶȱ��ֲ��䣬�����ж�ƽ�⣬�ʲ�ѡ��
d��A�İٷֺ������ֲ��䣬����������������Ϊƽ��״̬����ѡ��
e��������������֪��B��C�����ʵ���Ũ��֮��Ϊ1��2���ʲ�ѡ��
�ʴ�Ϊ��bd��
��2��������������֪��x=3����B��ʾ�÷�Ӧ��ƽ����Ӧ����V��B��=$\frac{\frac{0.4mol}{2L}}{2min}$=0.1 mol•L-1•min-1��
�ʴ�Ϊ��3��0.1 mol•L-1•min-1��
��3�������¶Ȳ��䣬�������������ѹǿ��С������Ӧ���ʼ�С���ʴ�Ϊ����С��
��4����ѧ��Ӧ�ﵽ��ʱ��A��ת����Ϊ$\frac{0.8mol}{2mol}$��100%=40%���ʴ�Ϊ��40%��
���� ���⿼�黯ѧƽ��ļ��㣬Ϊ��Ƶ���㣬����ƽ�����η������ʼ�ת���ʵļ��㡢ƽ���ж�Ϊ���Ĺؼ������ط�������������Ŀ��飬ע��x��ȷ����������Ŀ�ѶȲ���

| A�� | 1.00mol NaCl���NA��NaCl ���� | |
| B�� | ���³�ѹ�£�22.4LCl2������þ�۷�Ӧ��ת�Ƶĵ�����Ϊ2NA | |
| C�� | һ�������£�2.3gNa������O2��ȫ��Ӧ����3.6g����ʱʧȥ�ĵ�����Ϊ0.1NA | |
| D�� | 28g��ϩ�ͻ����飨C3H6����ɵĻ�������к�����ԭ�ӵĸ���Ϊ3 NA |
| A�� | ���� | B�� | ���� | C�� | ���� | D�� | ���������� |
������ʾ��FeCO3����ɫ�ᾧ��������ˮ������Ʒ�ڿ������ȶ���ʪƷ��¶�ڿ����л����������ɺ���ɫ��ˮ��������FeO��OH��
��1��ʵ��̽����
| ʵ �� �� | ���� | ���� |
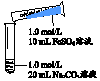 | 1����Ϻ���ְ�ɫ��״�����������ֳ����ʻ���ɫ�������ݲ��� 2������5-8���ӣ�����ɫ���������࣬���ձ�ɺ��ɫ |
�ڷ�Ӧ�����п�������Fe��OH��2�������ǰ�ɫ��״��ɻ���ɫ������ɺ��ɫ��
��ȡ�������ġ����ϴ�ӣ�������ϡ���ᣬ�����ܽ��������ݲ�����֤����ɫ�����к���CO32-����ʱ��Һ�д��ڵĽ�����������Fe3+��Fe2+��
��2��ʵ��̽����
| ʵ��� | ���� | ���� |
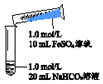 | 1����Ϻ��Թ��г��ְ�ɫ����״���ǣ�Ƭ�̺��д������ݲ��� 2����ճ�����Թ��ڱڵİ�ɫ����״���DZ����ɫ����Խ��Խ�ࣻ20���Ӻ�ɫ�������Գ��� |
�ڷ���������Ϊ��ʵ������ù�����FeCO3�ĺ�����ʵ���࣮֧�ָý��۵IJ������������£��ֱ����ֳ������Ĺ��ˡ�ϴ�ӡ�������ȡ�����������ֹ��壬������ϡ����������ܽ⣬ʵ����в����������ʵ����в��������������۳�����
��3��ʵ��̽����
| ʵ��� | ���� | ���� |
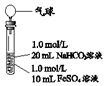 | 1����Ϻ��Թ��г��ְ�ɫ����״���ǣ�Ƭ�̺��д������ݲ��� 2��һ��ʱ����������ž��������Ľ��������Թܣ������5Сʱ���������ͣ��Թ��г�����ʼ�ձ��ְ�ɫ |
��4���ۺ�����ʵ�飬����˵����ȷ����ad
a����NaHCO3�Ƶ�FeCO3���ȸߵ�ԭ��֮һ����ΪNaHCO3��Һ������
b����1L 1.0mol/L NaHCO3������FeSO4��Һ��Ӧ�����Ͽ��Ʊ�116g FeCO3
c��ʪƷFeCO3�ڿ����л��������ķ���ʽΪ 4FeCO3+O2+6H2O=4Fe��OH��3+4CO2
d����ҵ����NH4HCO3��FeSO4��Ӧ���Ʊ����ȸ��ߵ�FeCO3��
�پ���ϩ���ϵ��ϻ�����Ϊ�����˼ӳɷ�Ӧ
��������ʳ��ƾ����˵��ۡ������ǡ��Ҵ��Ļ�ѧ�仯����
�۵��ۡ���֬����������һ�������¶��ܷ���ˮ�ⷴӦ
��ʯ�͵ķ����ú�ĸ����Ƿ����˻�ѧ�仯
�ݵ��ǡ����Ƕ���������Cu��OH��2������Ӧ
��������Һ�еμӱ���NaCl��Һ��CuSO4��Һ�����й���������
| A�� | �٢ڢۢܢ� | B�� | �ڢۢ� | C�� | �ڢۢܢ� | D�� | �ڢݢ� |
| A�� | �ơ�þ����ԭ�Ӱ뾶�������� | B�� | NH3H2O HF �ȶ������μ��� | ||
| C�� | H3PO4H2SO4HClO4����������ǿ | D�� | NaOH Mg��OH��2 Al��OH��3����������ǿ |
| A�� | ʯ�ͷ������õ������һ�־��й̶��۷е�Ĵ����� | |
| B�� | ʯ���ѻ�����ҪĿ����������͵������͵IJ��� | |
| C�� | ʯ���ѽ��ԭ����ʯ�ͷ���������ʯ���� | |
| D�� | ʯ�͵Ļ�ѧ�ɷ���Ҫ�Ǹ���Һ̬��̼�⻯������л�������̬��̬��̼�⻯���� |
| A�� | ��ѧ��ת���ɻ�е����ת���ɵ��� | |
| B�� | ��ѧ��ת����������ת���ɵ��� | |
| C�� | ��ѧ��ת���ɻ�е����ת���������ڵ���е�� | |
| D�� | ��ѧ��ת����������ת���ɻ�е���ڵ����� |