题目内容
9. 在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:
在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:C(s)+2NO(g)?CO2(g)+N2(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是( )
| A. | 在T2时,若反应体系处于状态D,则此时v正>v逆 | |
| B. | 若该反应在T1、T2时的平衡常数分别为K1、K2,则K1<K2 | |
| C. | 若状态B、C、D的压强分别为PB、PC、PD,则 PC=PD>PB | |
| D. | 该反应的△H>0 |
分析 A.由图可知,T2时反应进行到状态D,c(CO)高于平衡浓度,故反应向逆反应进行;
B.化学平衡常数只受温度影响,升高温度平衡向吸热反应移动,根据平衡移动判断温度对平衡常数的影响分析;
C.达到平衡状态时,压强和温度成正比例关系;
D.由图可知,温度越高平衡时c(NO)越大,即升高温度平衡逆移.
解答 解:A.T2时反应进行到状态D,c(NO)高于平衡浓度,故反应向正反应进行,则一定有υ(正)>υ(逆),故A正确;
B.该反应正反应是放热反应,升高温度平衡向逆反应移动,所以升温化学平衡常数减小,故K1>K2,故B错误;
C.达到平衡状态时,压强和温度成正比例关系,则PB=PD<PC,故C错误;
D.由图可知,温度越高平衡时c(NO)越大,即升高温度平衡逆移,所以正反应为放热反应,即△H<0,故D错误;
故选A.
点评 本题以化学平衡图象为载体,考查温度对平衡移动的影响、对化学平衡常数的影响等知识,题目难度中等,注意曲线的各点都处于平衡状态,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
20.下列反应中属于放热反应的是( )
| A. | Al与盐酸的反应 | |
| B. | 灼热的炭与二氧化碳反应生成一氧化碳 | |
| C. | 石灰石受热分解 | |
| D. | 水分解生成氧气和氢气 |
4.下列有关说法中正确的是( )
| A. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 | |
| B. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| C. | 目前科学家已经制得单原子层锗,其电子迁移率是硅的10倍,有望取代硅用于制造更好的晶体管 | |
| D. | 纤维素在人体内可水解为葡萄糖,是人类重要的营养物质之一 |
5.由于碳碳双键(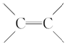 )不能自由旋转,因此
)不能自由旋转,因此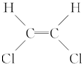 和
和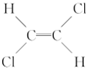 是两种不同的化合物,互为顺反异构体,则分子式为C4H7Cl的烯烃的异构体有( )
是两种不同的化合物,互为顺反异构体,则分子式为C4H7Cl的烯烃的异构体有( )
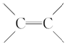 )不能自由旋转,因此
)不能自由旋转,因此 和
和 是两种不同的化合物,互为顺反异构体,则分子式为C4H7Cl的烯烃的异构体有( )
是两种不同的化合物,互为顺反异构体,则分子式为C4H7Cl的烯烃的异构体有( )| A. | 12种 | B. | 11种 | C. | 9种 | D. | 10种 |
12.能正确表示下列反应的离子方程式是( )
| A. | 碳酸钙溶于稀盐酸中:Ca2++2H+=Ca2++H2O+CO2↑ | |
| B. | 向氯化亚铁溶液中通入氯气:2Fe2++Cl2=2Fe3++2Cl- | |
| C. | Ba(OH)2与稀H2SO4反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| D. | 铜片跟稀硝酸反应:Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O |
9.某化学反应2A?B+D在四种不同条件下进行,B、D起始浓度均为0.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内A的平均速率为0.013mol/(L•min).
(2)在实验2,A的初始浓度c2=1.0mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是催化剂.
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3>v1(填>、=、<)
(4)比较实验4和实验1,可推测该反应是吸热反应(选填吸热、放热).请简述理由温度升高时,平衡向右移动.
| 实验序号 |  | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
(1)在实验1,反应在10至20分钟时间内A的平均速率为0.013mol/(L•min).
(2)在实验2,A的初始浓度c2=1.0mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是催化剂.
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3>v1(填>、=、<)
(4)比较实验4和实验1,可推测该反应是吸热反应(选填吸热、放热).请简述理由温度升高时,平衡向右移动.
 .
. ,它含有的化学键类型有AC(填序号).
,它含有的化学键类型有AC(填序号).
 .
.