题目内容
水果成熟时,大多数香气袭人.乙酸丁酯(CH3COOCH2CH2CH2CH3)是具有果香味的香精,经酯化反应可进行乙酸丁酯的合成.有关物质的物理性质见表.合成过程如下:第一步:将丁醇和x的混合液和过量的乙酸混合加热发生酯化反应;第二步:洗涤提纯;第三步:蒸馏提纯.

(1)如图是合成和提纯乙酸丁酯的有关装置图,请写出合成和提纯乙酸丁酯的操作顺序(填字母)C→F→ → → → .
(2)C装置中除了装有1-丁醇和过量的乙酸外,还装有 、 .装置C中冷凝管的作用是: ;
(3)乙酸过量的原因是 .
(4)步骤F:酯化反应完成后,向卸下的烧瓶中加入25mL水的作用是
(5)步骤E的操作要领是:①用一只手的手掌压住分液漏斗的塞子并握住分液漏斗;②另一只手握住活塞部分;③ .
(6)要除去乙酸丁酯中含有的少量乙酸,下列试剂中可选用的是:
A.饱和NaOH溶液 B.饱和KHCO3溶液 C.饱和Na2CO3溶液D.饱和 K2CO3溶液 E.饱和KOH溶液 F.过量的 1-丁醇.
| 乙酸 | 1-丁醇 | 乙酸丁酯 | |
| 熔点/℃ | 16.6 | -89.5 | -73.5 |
| 沸点/℃ | 117.9 | 117 | 126.3 |
| 密度/g?cm-3 | 1.05 | 0.81 | 0.88 |
| 水溶性 | 互溶 | 互溶 | 不溶 |

(1)如图是合成和提纯乙酸丁酯的有关装置图,请写出合成和提纯乙酸丁酯的操作顺序(填字母)C→F→
(2)C装置中除了装有1-丁醇和过量的乙酸外,还装有
(3)乙酸过量的原因是
(4)步骤F:酯化反应完成后,向卸下的烧瓶中加入25mL水的作用是
(5)步骤E的操作要领是:①用一只手的手掌压住分液漏斗的塞子并握住分液漏斗;②另一只手握住活塞部分;③
(6)要除去乙酸丁酯中含有的少量乙酸,下列试剂中可选用的是:
A.饱和NaOH溶液 B.饱和KHCO3溶液 C.饱和Na2CO3溶液D.饱和 K2CO3溶液 E.饱和KOH溶液 F.过量的 1-丁醇.
考点:乙酸乙酯的制取
专题:实验题
分析:(1)由乙酸丁酯的合成和提纯的步骤可知,反应装置为C,然后水洗为F、萃取为E、A装置进行水洗除去苯甲酸,选D过滤,最后蒸馏为B;
(2)反应装置中需要催化剂、沸石,C中冷凝管可使反应物冷凝回流;
(3)酯化反应为可逆反应,提高相对廉价的乙酸可以使平衡正向移动,提高了乙酸丁酯的产率;
(4)未反应的酸和醇易溶于水;
(5)步骤E为萃取操作,操作要领为:①用一只手的手掌压住分液漏斗的塞子并握住分液漏斗;②另一只手握住活塞部分③倒转分液漏斗反复振荡,并旋转活塞放出可能产生的气体;
(6)乙酸丁酯在强碱性溶液中可发生水解,乙酸乙酯溶于1-丁醇.
(2)反应装置中需要催化剂、沸石,C中冷凝管可使反应物冷凝回流;
(3)酯化反应为可逆反应,提高相对廉价的乙酸可以使平衡正向移动,提高了乙酸丁酯的产率;
(4)未反应的酸和醇易溶于水;
(5)步骤E为萃取操作,操作要领为:①用一只手的手掌压住分液漏斗的塞子并握住分液漏斗;②另一只手握住活塞部分③倒转分液漏斗反复振荡,并旋转活塞放出可能产生的气体;
(6)乙酸丁酯在强碱性溶液中可发生水解,乙酸乙酯溶于1-丁醇.
解答:
解:(1)由乙酸丁酯的合成和提纯的步骤可知,反应装置为C,然后水洗为F、萃取为E、A装置进行水洗除去苯甲酸,选D过滤,最后蒸馏为B,则实验装置的顺序为C→F→E→A→D→B,故答案为:E;A;D;B;
(2)C中除了装有1-丁醇和过量的乙酸外,还需要浓硫酸作催化剂,需要沸石防止暴沸,C中加热,反应物转化为气体,则冷凝管可使挥发的乙酸和丁醇冷凝回流,
故答案为:浓硫酸;沸石;使挥发的乙酸和丁醇冷凝回流;
(3)酯化反应为可逆反应,提高相对廉价的乙酸可以使平衡正向移动,提高了乙酸丁酯的产率,故答案为:提高乙酸丁酯的产率;
(4)未反应的酸和醇易溶于水,向卸下的烧瓶中加入25mL水的作用是溶解吸收未反应的酸和醇,故答案为:溶解吸收未反应的酸和醇;
(5)步骤E为萃取操作,操作要领为:①用一只手的手掌压住分液漏斗的塞子并握住分液漏斗;②另一只手握住活塞部分③倒转分液漏斗反复振荡,并旋转活塞放出可能产生的气体,
故答案为:倒转分液漏斗反复振荡,并旋转活塞放出可能产生的气体;
(6)乙酸丁酯在强碱性溶液中可发生水解,因此AE不选,乙酸乙酯溶于1-丁醇,且引入了新的杂质,因此F不选,饱和KHCO3溶液、饱和Na2CO3溶液、饱和 K2CO3溶液水解均呈弱碱性,可以中和乙酸,且可以降低乙酸丁酯的溶解度,
故答案为:BCD.
(2)C中除了装有1-丁醇和过量的乙酸外,还需要浓硫酸作催化剂,需要沸石防止暴沸,C中加热,反应物转化为气体,则冷凝管可使挥发的乙酸和丁醇冷凝回流,
故答案为:浓硫酸;沸石;使挥发的乙酸和丁醇冷凝回流;
(3)酯化反应为可逆反应,提高相对廉价的乙酸可以使平衡正向移动,提高了乙酸丁酯的产率,故答案为:提高乙酸丁酯的产率;
(4)未反应的酸和醇易溶于水,向卸下的烧瓶中加入25mL水的作用是溶解吸收未反应的酸和醇,故答案为:溶解吸收未反应的酸和醇;
(5)步骤E为萃取操作,操作要领为:①用一只手的手掌压住分液漏斗的塞子并握住分液漏斗;②另一只手握住活塞部分③倒转分液漏斗反复振荡,并旋转活塞放出可能产生的气体,
故答案为:倒转分液漏斗反复振荡,并旋转活塞放出可能产生的气体;
(6)乙酸丁酯在强碱性溶液中可发生水解,因此AE不选,乙酸乙酯溶于1-丁醇,且引入了新的杂质,因此F不选,饱和KHCO3溶液、饱和Na2CO3溶液、饱和 K2CO3溶液水解均呈弱碱性,可以中和乙酸,且可以降低乙酸丁酯的溶解度,
故答案为:BCD.
点评:本题考查混合物分离、提纯实验的方案和设计,为高频考点,把握物质的性质及实验流程为解答的关键,侧重分析、实验能力的考查,题目难度中等.

练习册系列答案
相关题目
下列有关物质的量的理解正确的是( )
| A、物质的量和摩尔是两个不同的物理量 |
| B、摩尔是物质的量的单位,1摩尔任何物质含6.02x1023个原子 |
| C、阿伏伽德罗常数是人们规定的数,没有单位 |
| D、当H2的摩尔质量以g.mol-1为单位时,在数值上与H2的相对分子质量相等 |
下列离子方程式与所述事实相符且正确的是( )
| A、0.5 mol/L NaHSO4与0.5 mol/L Ba(OH)2混合至溶液呈中性:Ba2++OH-+SO42-+H+═BaSO4↓+H2O |
| B、向2 mol/L Fe(NO3)2(aq)中滴加少量氢碘酸:3Fe2++NO3-+4H+═3Fe3++NO↑+2H2O |
| C、向20 mL0.15 mol/L氢碘酸中通入224 mL Cl2(标准状况):2HI+Cl2═2H++I2+2Cl- |
| D、向40 mL 0.5 mol/L NaOH(aq)中通入224 mL CO2(标准状况):2OH-+CO2═CO32-+H2O |
将过量的CO2通入下列溶液中,最终会出现浑浊的是( )
| A、CaCl2溶液 |
| B、NaAlO2溶液 |
| C、Na2CO3溶液 |
| D、水玻璃 |
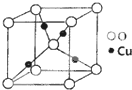 某催化剂中含有的活性组分为Ni、Cu和Zn的化合物,可用于二氧化碳加氢制取甲醚.甲醚是乙醇的同分异构体,其熔点-141.5℃,沸点-24.9℃,在加热条件下可分解成甲烷、乙烷、甲醛等.
某催化剂中含有的活性组分为Ni、Cu和Zn的化合物,可用于二氧化碳加氢制取甲醚.甲醚是乙醇的同分异构体,其熔点-141.5℃,沸点-24.9℃,在加热条件下可分解成甲烷、乙烷、甲醛等.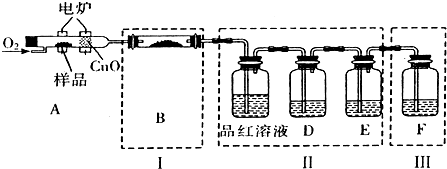
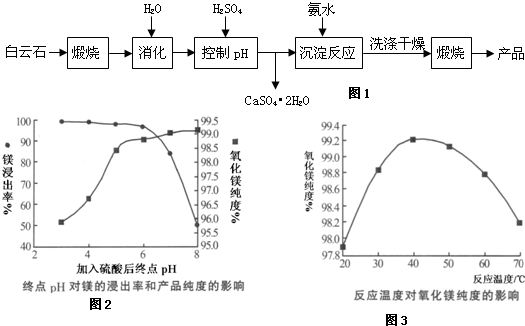
 如图在甲处的试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入5mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在乙处的试管中加入5mL饱和碳酸钠溶液,按图连接好装置,用酒精灯对甲处的试管缓慢加热,当观察到乙处的试管中有明显现象时停止实验.请回答:
如图在甲处的试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入5mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在乙处的试管中加入5mL饱和碳酸钠溶液,按图连接好装置,用酒精灯对甲处的试管缓慢加热,当观察到乙处的试管中有明显现象时停止实验.请回答: