题目内容
15.NaCl、NaClO、NaClO3的混合物中,已知Na的质量分数为23%,则氧元素的质量分数为( )| A. | 21.5% | B. | 45.1% | C. | 31.0% | D. | 41.5% |
分析 由混合物可知,Na、Cl的质量比为23:35.5,三种元素的质量分数之和为1,以此来解答.
解答 解:由混合物可知,Na、Cl的质量比为23:35.5,由Na的质量分数为23%,则Cl元素的质量分数为35.5%,则氧元素的质量分数为1-23%-35.5%=41.5%,
故选D.
点评 本题考查元素质量分数的计算,为高频考点,把握物质的定组成为解本题关键,侧重分析与计算能力的考查,注意三种元素的质量分数之和为1,题目难度不大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
6.下列反应的离子方程式正确的是( )
| A. | 碳酸钙与盐酸的反应:CO32-+2H+═CO2↑+H2O | |
| B. | 硫酸与氢氧化钠溶液的反应:H++OH-═H2O | |
| C. | 硝酸银与氯化钠溶液的反应:AgNO3+Cl-═AgCl↓+NO3- | |
| D. | 铝与硫酸铜溶液的反应:Al+Cu2+═Al3++Cu |
10.下列实验能获得成功的是( )
①用醋酸钠晶体和碱石灰共热制取甲烷;②将甲烷气体通入溴水中制取溴甲烷;③用酒精灯加热CH4制取炭黑和氢气;④将甲烷气体与溴蒸气混合光照制取纯净的一溴甲烷;⑤用电石和饱和食盐水制取乙炔;⑥用酒精和稀硫酸混合加热至170℃制取乙烯.
①用醋酸钠晶体和碱石灰共热制取甲烷;②将甲烷气体通入溴水中制取溴甲烷;③用酒精灯加热CH4制取炭黑和氢气;④将甲烷气体与溴蒸气混合光照制取纯净的一溴甲烷;⑤用电石和饱和食盐水制取乙炔;⑥用酒精和稀硫酸混合加热至170℃制取乙烯.
| A. | ①②③ | B. | ④⑤⑥ | C. | ⑤ | D. | ④⑥ |
20.下列叙述正确的是( )
| A. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 | |
| B. | 分离乙醇和乙酸乙酯的混合物需要的玻璃仪器为分液漏斗和烧杯 | |
| C. | 从碘水中提取单质碘时,不能用无水乙醇代替CCl4 | |
| D. | 先加入碘水,再加入CCl4,振荡后静置,液体分层,下层呈无色 |
7.下列分离或提纯物质的方法正确的是( )
| A. | 用过滤的方法除去NaCl溶液中含有的少量KCl | |
| B. | 用蒸馏的方法制取蒸馏水 | |
| C. | 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 | |
| D. | 用加热、蒸发的方法可以除去CaCl2、MgCl2等杂质 |
10.用下列实验装置和方法进行相应实验,正确的是( )
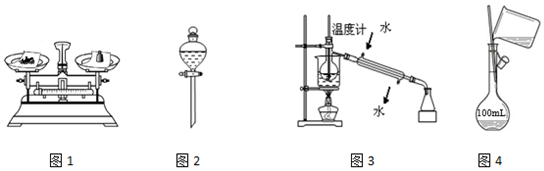

| A. | 用图1所示方法称量固体氯化钠 | |
| B. | 用图2装置分离碘的四氯化碳溶液 | |
| C. | 用图3所示装置和方法进行石油分馏 | |
| D. | 用图4装置配制150 mL稀盐酸 |