题目内容
17.对于以下三个反应,从正向开始进行达到平衡后,保持温度、体积不变,按要求回答下列问题.PCl5(g)?PCl3(g)+Cl2(g)
再充入PCl5(g)平衡向逆向方向移动,达到平衡后,PCl5(g)的转化率减小,PCl5(g)的百分含量增大.
分析 保持温度、体积不变,再充入PCl5(g),n增大,则压强增大,结合压强对平衡移动的影响来解答.
解答 解:保持温度、体积不变,再充入PCl5(g),n增大,则压强增大,该反应为气体体积增大的反应,则增大压强平衡逆向移动,PCl5(g)的转化率减小,PCl5(g)的百分含量增大,
故答案为:逆向;减小;增大.
点评 本题考查化学平衡移动,为高频考点,把握体积不变时物质的量与压强的关系为解答的关键,侧重分析与应用能力的考查,注意压强对平衡移动的影响,题目难度不大.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
5.把铝片放入盛有过量稀硫酸的试管中,下列措施不能加快产生氢气的速率的是( )
| A. | 把稀硫酸换为浓硫酸 | B. | 把铝片换成镁片 | ||
| C. | 加入少量CuSO4溶液 | D. | 加少量NaHSO4固体 |
12.实验是进行化学研究的重要环节,下列有关化学实验的说法正确的是( )
| A. | 向滴有KSCN的FeCl3溶液中加入NaOH溶液以研究反应物浓度对化学平衡的影响 | |
| B. | 用酒精萃取碘水中的碘,水从分液漏斗下口放出,碘的酒精溶液从分液漏斗上口倒出 | |
| C. | 将高锰酸钾溶液装入碱式滴定管中进行滴定实验,以测定某FeSO4样品的纯度 | |
| D. | 为制备硅酸胶体,以酚酞为指示剂,将浓盐酸滴入饱和Na2SiO3溶液中 |
2.下列实验方案能达到实验目的是( )
| 选项 | 实验方案 | 实验目的 |
| A | 镁和铝在烧碱溶液中构成原电池 | 证明镁比铝活泼 |
| B | 向锌和稀硫酸的混合物中加入大量硫酸铜溶液 | 加快产生氢气速率 |
| C | 以铁为电极,电解次氯酸钠和氢氧化钠的混合溶液 | 制备白色氢氧化亚铁 |
| D | 用石墨为电极,电解浓度都为0.1mol•L-1的硝酸铜和硝酸银的混合溶液 | 探究Cu2+和Ag+的氧化性强弱 |
| A. | A | B. | B | C. | C | D. | D |
9.下列说法正确的是( )
| A. | 0.1 mol•L-1 Na2CO3溶液中:c(HCO3-)=2c(H2CO3 )+c(H+)-c(OH-) | |
| B. | pH=5 的 NaHSO3 溶液中:c(H2SO3)>c(SO32- ) | |
| C. | 同浓度的下列溶液中,①NH4HSO4 ②NH4Cl③NH3•H2O,c(NH4-)由大到小的顺序是:②>①>③ | |
| D. | 常温下,pH=3 的 CH3COOH 溶液和 pH=11 的 NaOH 溶液等体积混合 c(CH3COO-)>c(Na +)>c(H+)>c(OH-) |
6.下列有关甲苯的说法中,不正确的是( )
| A. | 可以与溴水发生取代反应 | B. | 可以与氢气发生加成反应 | ||
| C. | 可以制造烈性炸药TNT | D. | 可以被酸性高锰酸钾溶液氧化 |
15.NaCl、NaClO、NaClO3的混合物中,已知Na的质量分数为23%,则氧元素的质量分数为( )
| A. | 21.5% | B. | 45.1% | C. | 31.0% | D. | 41.5% |
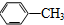 E.
E.