题目内容
 以葡萄糖为燃料的微生物燃料电池如图所示.关于该电池的叙述正确的是( )
以葡萄糖为燃料的微生物燃料电池如图所示.关于该电池的叙述正确的是( )| A、该电池能够在高温下工作 |
| B、电池的负极反应为:C6H12O6+6H2O-24e-=6CO2↑+24H+ |
| C、放电过程中,将生成的CO2和水随时排出,保持电解质浓度恒定 |
| D、在电池反应中,每消耗1mol氧气,理论上能生成标准状况下CO222.4/6 L |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、从蛋白质的性质分析;
B、负极是葡萄糖失电子生成二氧化碳,电极反应为C6H12O6+6H2O-24e-=6CO2↑+24H+;
C、根据电池的电极反应和总反应知识来回答;
D、根据正负极电极反应式结合电子守恒原理进行计算.
B、负极是葡萄糖失电子生成二氧化碳,电极反应为C6H12O6+6H2O-24e-=6CO2↑+24H+;
C、根据电池的电极反应和总反应知识来回答;
D、根据正负极电极反应式结合电子守恒原理进行计算.
解答:
解:A、高温条件下微生物会变性,该电池不能够在高温下工作,故A错误;
B、负极是葡萄糖失电子生成二氧化碳,电极反应为C6H12O6+6H2O-24e-=6CO2↑+24H+,故B正确;
C、该电池的反应产物是水以及二氧化碳,将生成的CO2和水随时排出,可以保持电解质浓度恒定,故C正确;
D、正极反应式为O2+4e-+4H+═2H2O,对比负极反应可知,消耗1mol氧气生成1mol二氧化碳,标准状况下体积是22.4L,故D错误;
故选BC.
B、负极是葡萄糖失电子生成二氧化碳,电极反应为C6H12O6+6H2O-24e-=6CO2↑+24H+,故B正确;
C、该电池的反应产物是水以及二氧化碳,将生成的CO2和水随时排出,可以保持电解质浓度恒定,故C正确;
D、正极反应式为O2+4e-+4H+═2H2O,对比负极反应可知,消耗1mol氧气生成1mol二氧化碳,标准状况下体积是22.4L,故D错误;
故选BC.
点评:本题从两个角度考查①原电池反应(反应原理、电极方程式的书写、离子的移动方向);②有关化学方程式的计算.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列离子方程式书写正确的是( )
| A、FeCl2溶液中通入Cl2:Fe2++Cl2=Fe3++2Cl- |
| B、过量CO2通入氢氧化钠溶液中:CO2+2OH-=CO32-+H2O |
| C、澄清石灰水与少量小苏打溶液混合:Ca2+十OH-+HCO3-=CaCO3↓+H2O |
| D、AlCl3溶液中加入过量氨水:Al3++4OH-=AlO2-+2H2O |
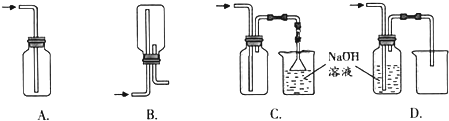
实验室进行下列有关物质的准备,理论上正确、操作上可行、经济上合理的是( )
A、C
| ||||||
B、Cu
| ||||||
C、CaO
| ||||||
D、Fe
|
下列离子方程式书写正确的是( )
| A、铝单质与NaOH溶液反应:2Al+2OH-=2AlO2-+3H2↑ |
| B、醋酸溶液与NaHCO3溶液反应:H++HCO3-=CO2↑+H2O |
| C、SO2通入溴水中:SO2+Br2+H2O=SO42-+2Br-+2H+ |
| D、铁溶于过量稀硝酸中:Fe+4H++NO3-=Fe3++NO↑+2H2O |
对硫酸溶于魔酸中所表现出的性质的叙述正确的是( )
| A、表现出强酸性 |
| B、表现出弱酸性 |
| C、表现出碱性 |
| D、1mol H2SO4可电离出2mol H+ |
NA代表阿伏加德罗常数的数值,下列说法正确的是(C-12 H-1)( )
| A、4.0g CH4中含有共价键的数目为NA |
| B、标准状况下,22.4L氨水含有NA个NH3分子 |
| C、常温下,0.1mol/L NH4NO3溶液中NO3-的数目为0.1NA |
| D、标准状况下,2.24L Cl2通入足量NaOH溶液中,反应转移电子的数目为0.2NA |
在一定温度下,某浓度的HNO3与Zn反应,生成NO2和NO的物质的量之比为1:3,则要使1mol Zn完全反应,需要HNO3的物质的量为( )
| A、2.8mol |
| B、2.6mol |
| C、2.4mol |
| D、0.8mol |