题目内容
下列离子检验方法合理的是( )
| A、向某溶液中滴入盐酸产生的气体能使澄清石灰水变浑浊,则溶液中含有CO32- |
| B、向某溶液中滴入KSCN溶液变为血红色,则溶液中一定含有Fe3+ |
| C、向某溶液中滴加硝酸酸化的BaCl2溶液,若产生白色沉淀,则溶液中一定含有SO42- |
| D、某溶液中通入CO2产生白色沉淀,则溶液中一定含有SiO32- |
考点:常见阴离子的检验,常见阳离子的检验
专题:物质检验鉴别题
分析:A、能使澄清石灰水变浑浊的气体可以是二氧化碳或二氧化硫,据此分析;
B、铁离子与KSCN发生络合反应生成血红色;
C、氯化钡与硫酸盐可以生成硫酸钡(难溶于稀硝酸的白色沉淀),也可以与硝酸银生成氯化银(难溶于稀硝酸的白色沉淀)沉淀;
D、碳酸的酸性强于硅酸、偏铝酸、苯酚,据此解答.
B、铁离子与KSCN发生络合反应生成血红色;
C、氯化钡与硫酸盐可以生成硫酸钡(难溶于稀硝酸的白色沉淀),也可以与硝酸银生成氯化银(难溶于稀硝酸的白色沉淀)沉淀;
D、碳酸的酸性强于硅酸、偏铝酸、苯酚,据此解答.
解答:
解:A、能使澄清石灰水变浑浊的气体可以是二氧化碳或二氧化硫,故原溶液中可能含有:CO32-、HCO3-、SO32-、HSO3-,故A错误;
B、铁离子与KSCN发生络合反应生成血红色,故原溶液中一定含有铁离子,故B正确;
C、氯化钡与硫酸盐可以生成硫酸钡难溶于稀硝酸的白色沉淀,也可以与硝酸银生成氯化银沉淀,故可能含有SO42-或者Ag+,故C错误;
D、碳酸的酸性强于硅酸、偏铝酸、苯酚,故原溶液中可能含有硅酸跟、偏铝酸根等,故D错误,
故选B.
B、铁离子与KSCN发生络合反应生成血红色,故原溶液中一定含有铁离子,故B正确;
C、氯化钡与硫酸盐可以生成硫酸钡难溶于稀硝酸的白色沉淀,也可以与硝酸银生成氯化银沉淀,故可能含有SO42-或者Ag+,故C错误;
D、碳酸的酸性强于硅酸、偏铝酸、苯酚,故原溶液中可能含有硅酸跟、偏铝酸根等,故D错误,
故选B.
点评:本题主要考查的是溶液中阴离子以及阳离子的检验,排除一些同等现象离子的干扰是解决本题的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
以下说法不正确的是( )
| A、误食重金属盐可立即服用大量的牛奶或豆浆解毒 |
| B、对生活中的塑料垃圾进行填埋,可防止“白色污染” |
| C、食用含铁丰富的食物,可改善贫血症状 |
| D、将碗筷高温蒸煮,可杀菌消毒 |
检验小苏打粉末中是否有苏打的方法是( )
| A、溶于水,加Ca(OH)2溶液 |
| B、溶于水,加稀CaCl2溶液 |
| C、加稀盐酸 |
| D、溶于水,加入NaOH溶液 |
5℃时,1mol?L-1的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2的溶液中,测得各溶液的c(NH4+)分别为a、b、c(单位为mol?L-1),下列判断正确的是( )
| A、a=b=c |
| B、a>b>c |
| C、a>c>b |
| D、c>a>b |
在一定条件下,发生CO(g)+NO2(g)?CO2(g)+NO(g)(正反应为放热反应)的反应,达到平衡后,保持体积不变,降低温度,混合气体的颜色( )
| A、变深 | B、先变深后变浅 |
| C、不变 | D、变浅 |

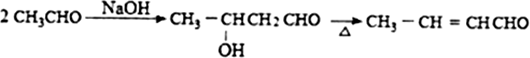
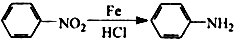 :苯胺中氨基易被氧化.
:苯胺中氨基易被氧化.