题目内容
下面是几种实验中常用的仪器:
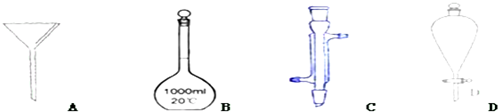
(1)写出序号所代表的仪器的名称:
B ;C ;D .
实验室要配制480mL 0.2mol/L NaOH溶液,请回答下列问题:
(2)用托盘天平称取氢氧化钠,其质量为 g.
(3)下列主要操作步骤的正确顺序是 (填序号).
①称取一定质量的氢氧化钠,放入烧杯中,用适量蒸馏水溶解;
②“定容”;
③待冷却至室温后,将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量的蒸馏水洗涤烧杯内壁和玻璃棒2-3次,洗涤液转移到容量瓶中.
(4)在配制过程中,其他操作都是正确的,下列操作会引起所配浓度偏高的是 .
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
(5)写出步骤②“定容”的具体操作: .

(1)写出序号所代表的仪器的名称:
B
实验室要配制480mL 0.2mol/L NaOH溶液,请回答下列问题:
(2)用托盘天平称取氢氧化钠,其质量为
(3)下列主要操作步骤的正确顺序是
①称取一定质量的氢氧化钠,放入烧杯中,用适量蒸馏水溶解;
②“定容”;
③待冷却至室温后,将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量的蒸馏水洗涤烧杯内壁和玻璃棒2-3次,洗涤液转移到容量瓶中.
(4)在配制过程中,其他操作都是正确的,下列操作会引起所配浓度偏高的是
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
(5)写出步骤②“定容”的具体操作:
考点:配制一定物质的量浓度的溶液
专题:
分析:(1)根据仪器的图形判断仪器的名称;
(2)依据m=CVM计算需要氢氧化钠的质量;
(3)依据配制一定物质的量浓度溶液的一般步骤排序;
(4)分析不当操作对溶质的物质的量和溶液的体积的影响,依据C=
进行误差分析;
(5)根据定容的正确操作解答.
(2)依据m=CVM计算需要氢氧化钠的质量;
(3)依据配制一定物质的量浓度溶液的一般步骤排序;
(4)分析不当操作对溶质的物质的量和溶液的体积的影响,依据C=
| n |
| V |
(5)根据定容的正确操作解答.
解答:
解:(1)由仪器的图形可知A为漏斗,B为1000mL容量瓶,C为冷凝管,D为分液漏斗;
故答案为:1000mL容量瓶;冷凝管;分液漏斗;
(2)配制480mL 0.2mol/L NaOH溶液,应选择500ml容量瓶,需要溶质的质量m=0.2mol/L×0.5L×40g/mol=4.0g;
故答案为:4.0;
(3)配制一定物质的量浓度溶液的一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀,所以正确的顺序:①③⑤②④;
故答案为:①③⑤②④;
(4)①没有洗涤烧杯和玻璃棒,导致溶质的物质的量偏小,溶液的浓度偏低,故①不选;
②转移溶液时不慎有少量洒到容量瓶外面,导致溶质的物质的量偏小,溶液的浓度偏低,故②不选;
③容量瓶不干燥,含有少量蒸馏水,对 溶质的物质的量和溶液的体积都不会产生影响,溶液的浓度不变,故③不选;
④定容时俯视刻度线,导致溶液的体积偏小,溶液的浓度偏高,故④选;
⑤未冷却到室温就将溶液转移到容量瓶并定容,冷却后溶液的体积偏小,溶液的浓度偏高,故⑤选;
故选:④⑤;
(5)定容的具体操作是:加水至液面离容量瓶颈刻度线1-2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
故答案为:加水至液面离容量瓶颈刻度线1-2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切.
故答案为:1000mL容量瓶;冷凝管;分液漏斗;
(2)配制480mL 0.2mol/L NaOH溶液,应选择500ml容量瓶,需要溶质的质量m=0.2mol/L×0.5L×40g/mol=4.0g;
故答案为:4.0;
(3)配制一定物质的量浓度溶液的一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀,所以正确的顺序:①③⑤②④;
故答案为:①③⑤②④;
(4)①没有洗涤烧杯和玻璃棒,导致溶质的物质的量偏小,溶液的浓度偏低,故①不选;
②转移溶液时不慎有少量洒到容量瓶外面,导致溶质的物质的量偏小,溶液的浓度偏低,故②不选;
③容量瓶不干燥,含有少量蒸馏水,对 溶质的物质的量和溶液的体积都不会产生影响,溶液的浓度不变,故③不选;
④定容时俯视刻度线,导致溶液的体积偏小,溶液的浓度偏高,故④选;
⑤未冷却到室温就将溶液转移到容量瓶并定容,冷却后溶液的体积偏小,溶液的浓度偏高,故⑤选;
故选:④⑤;
(5)定容的具体操作是:加水至液面离容量瓶颈刻度线1-2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
故答案为:加水至液面离容量瓶颈刻度线1-2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切.
点评:本题考查一定物质的量浓度溶液的配制,明确配制过程和原理是解题关键,注意误差分析的方法.

练习册系列答案
相关题目
有关食品添加剂的下列说法中正确的是( )
| A、食盐加碘,碘元素百分含量越高,食盐的质量越高 |
| B、菜炒熟出锅前再放碘盐以防分解,加醋会降低碘的利用率 |
| C、苯甲酸钠是常用的食品调味剂 |
| D、腌制肉食制品使用的亚硝酸盐即使不超标,也不可长期或大量的进食 |
甲醛(HCHO)是一种致癌物,下列有关甲醛的使用不会影响人体健康的是( )
| A、用经甲醛处理过的胶合板装修居室 |
| B、用甲醛处理过的衬衫具有免熨效果 |
| C、将生物标本浸于盛有甲醛水溶液的密封瓶中 |
| D、海产品用甲醛水溶液浸泡,以保鲜防腐 |
下列离子检验方法合理的是( )
| A、向某溶液中滴入盐酸产生的气体能使澄清石灰水变浑浊,则溶液中含有CO32- |
| B、向某溶液中滴入KSCN溶液变为血红色,则溶液中一定含有Fe3+ |
| C、向某溶液中滴加硝酸酸化的BaCl2溶液,若产生白色沉淀,则溶液中一定含有SO42- |
| D、某溶液中通入CO2产生白色沉淀,则溶液中一定含有SiO32- |
将铁、铝的混合物加入到足量的NaOH溶液中,使之充分反应后过滤,再将过滤得到的固体加入到足量的CuSO4溶液中,充分反应后过滤得到的固体质量恰好与原固体质量相等,则原固体中铁的质量分数为( )
| A、87.5% |
| B、12.5% |
| C、14.3% |
| D、85.7% |
下列说法正确的是( )
| A、有化学键破坏的变化一定属于化学变化 |
| B、化学反应过程中,某离子被沉淀完全时,该离子在溶液中的浓度即为0 |
| C、形成化学键吸收能量,破坏化学键释放能量 |
| D、若化学平衡向正方向移动,则正反应速率不一定增大 |
现有等体积的Ba(OH)2、NaOH和NH3?H2O三种溶液,将它们分别与V1L、V2L、V3L等浓度的盐酸混合,下列说法中正确的是( )
| A、若混合前三溶液的物质的量浓度相等,混合后溶液呈中性,则V1>V2>V3 |
| B、若混合前三溶液的pH相等,酸碱恰好完全反应,则V1>V2>V3 |
| C、若混合前三溶液的物质的量浓度相等,酸碱恰好完全反应,则V1>V2>V3 |
| D、若混合前三溶液的pH相等,将它们同等倍数稀释后,则NaOH溶液pH最大 |

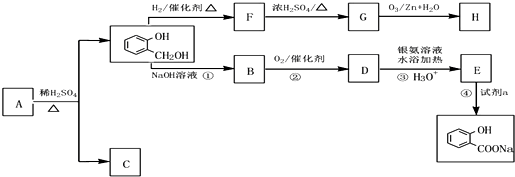
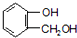 到F反应是否进行完全,可用FeCl3溶液检验
到F反应是否进行完全,可用FeCl3溶液检验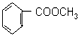 的最佳路线流程图(无机试剂任选).
的最佳路线流程图(无机试剂任选).