题目内容
7.下列与有机物有关的说法,错误的是( )| A. | 乙烯和甲烷可用溴的四氯化碳溶液鉴别 | |
| B. | 甲烷、苯、乙酸都可以发生取代反应 | |
| C. | 标况下,1mol 乙醇可与足量的Na反应生成22.4LH2 | |
| D. | 乙酸可与Na2CO3溶液反应生成CO2 |
分析 A.乙烯可与溴的四氯化碳发生加成反应;
B.甲烷可与氯气发生取代反应,苯可与溴、浓硝酸等发生取代反应,乙酸可与乙醇发生取代反应;
C.乙醇含有1个羟基;
D.乙酸的酸性比碳酸强.
解答 解:A.乙烯可与溴的四氯化碳发生加成反应,而甲烷不反应,可用溴的四氯化碳溶液鉴别,故A正确;
B.甲烷可与氯气在光照条件下发生取代反应,苯可与溴、浓硝酸等在催化条件下发生取代反应,乙酸可与乙醇发生酯化反应,也为取代反应,故B正确;
C.乙醇含有1个羟基,标况下,1mol 乙醇可与足量的Na反应生成11.2H2,故C错误;
D.乙酸的酸性比碳酸强,可与碳酸钠反应生成二氧化碳气体,故D正确.
故选C.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的官能团的性质,难度不大.

练习册系列答案
 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
12.在理论上不能用于设计原电池的化学反应是( )
| A. | 2H2(g)+O2(g)=2H2O(l)△H<0 | B. | 2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H<0 | ||
| C. | HCl(aq)+NaOH (aq)=NaCl(aq)+H2O(l)△H<0 | D. | 4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe (OH)3(s)△H<0 |
16.下列物质中,可用于制造光导纤维的是( )
| A. | 铜合金 | B. | 陶瓷 | C. | 纤维素 | D. | 二氧化硅 |
17.苹果酸( )易溶于水,常用做汽水,糖果的添加剂.下列有关说法中,正确的是( )
)易溶于水,常用做汽水,糖果的添加剂.下列有关说法中,正确的是( )
 )易溶于水,常用做汽水,糖果的添加剂.下列有关说法中,正确的是( )
)易溶于水,常用做汽水,糖果的添加剂.下列有关说法中,正确的是( )| A. | 苹果酸属于烃 | B. | 苹果酸中有3种官能团 | ||
| C. | 苹果酸的分子式是C3H6O5 | D. | 苹果酸能使紫色石蕊溶液变红 |

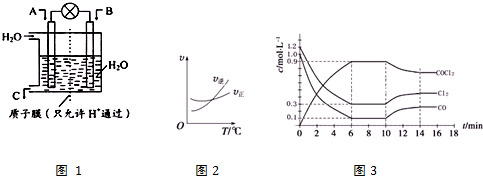
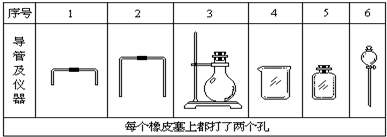
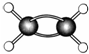 科学家致力于二氧化碳的“组合转化”技术的研究,把过多二氧化碳转化为有益于人类的物质.
科学家致力于二氧化碳的“组合转化”技术的研究,把过多二氧化碳转化为有益于人类的物质. 代表氢原子,
代表氢原子, 代表碳原子)和水,该有机物的结构简式为CH2=CH2.
代表碳原子)和水,该有机物的结构简式为CH2=CH2.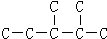 ,该烷烃的名称为2,3-二甲基戊烷;其一溴代物有6种.
,该烷烃的名称为2,3-二甲基戊烷;其一溴代物有6种.