题目内容
3.取两份100ml Na2CO3溶液与两份50ml 1mol/L的盐酸,在不断搅拌下,将Na2CO3溶液逐滴滴入盐酸中与将盐酸逐滴滴入Na2CO3溶液中,所产生的气体物质的量之比为5:2.则Na2CO3溶液的物质的量浓度为( )| A. | 0.2 mol/L | B. | 0.32 mol/L | C. | 0.4 mol/L | D. | 0.5 mol/L |
分析 将碳酸钠溶液逐滴滴入盐酸中,盐酸过量,发生反应是Na2CO3+2HCl=2NaCl+CO2↑+H2O,将盐酸逐滴滴入碳酸钠溶液中,碳酸钠过量,首先发生的反应是Na2CO3+HCl=NaHCO3+NaCl,碳酸钠反应完后,再发生反应是NaHCO3+HCl=NaCl+CO2+H2O;
如果对两个过程,盐酸都过量,则两次产生CO2应该一样多,但两者不同,说明在第一个过程中盐酸完全反应,碳酸钠有剩余,第二过程中盐酸也完全反应,但有碳酸氢钠剩余.
根据HCl的物质的量计算第一个过程的二氧化碳的物质的量,进而计算第二个过程生成二氧化碳的物质的量,根据方程式:NaHCO3+HCl=NaCl+CO2+H2O计算参加该反应的HCl的物质的量,进而计算反应:Na2CO3+HCl=NaHCO3+NaCl中消耗的HCl的物质的量,据此计算Na2CO3的物质的量,再根据c=$\frac{n}{V}$计算.
解答 解:将碳酸钠溶液逐滴滴入盐酸中,盐酸过量,发生反应是Na2CO3+2HCl=2NaCl+CO2↑+H2O,将盐酸逐滴滴入碳酸钠溶液中,碳酸钠过量,首先发生的反应是Na2CO3+HCl=NaHCO3+NaCl,碳酸钠反应完后,再发生反应是NaHCO3+HCl=NaCl+CO2+H2O;如果对两个过程,盐酸都过量,则两次产生CO2应该一样多,但两者不同,说明在第一个过程中盐酸完全反应,碳酸钠有剩余,第二过程中盐酸也完全反应,但有碳酸氢钠剩余,
n(HCl)=0.05L×1mol/L=0.05mol,故第一个过程生成二氧化碳为0.05mol×$\frac{1}{2}$=0.025mol,则第二个过程生成二氧化碳为0.025mol×$\frac{2}{5}$=0.01mol,故反应NaHCO3+HCl=NaCl+CO2+H2O中消耗的HCl为0.01mol,反应Na2CO3+HCl=NaHCO3+NaCl中消耗的HCl为0.05mol-0.01mol=0.04mol,故碳酸钠的物质的量为0.04mol,物质的量浓度为$\frac{0.04mol}{0.1L}$=0.4mol/L,故选C.
点评 本题考查方程式的有关计算,清楚滴加顺序不同发生的反应,判断向盐酸中滴加碳酸钠盐酸完全反应是关键.

| A. | 1 mol苯乙烯可以和4mol Br2发生加成反应 | |
| B. | 分子中所有原子可以在同一平面内 | |
| C. | 与HCl加成只生成一种产物 | |
| D. | 能使酸性KMnO4溶液褪色 |
①NH4HCO3
②NH3
③BaSO4;
④CH3COONa•3H2O
⑤Ba(OH)2
⑥H2SO4.
| A. | ①④⑥ | B. | ②③⑤ | C. | ④⑤ | D. | ②⑥ |
| A. | 0.1mol/L | B. | 0.2mol/L | C. | 0.3mol/L | D. | 0.4mol/L |
| A. | 江河入海口三角洲的形成通常与胶体的性质有关 | |
| B. | 往Fe(OH)3胶体中逐滴加入稀硫酸会产生沉淀而后沉淀逐渐溶解 | |
| C. | 纳米材料粒子直径一般从几纳米到几十纳米,因此纳米材料属于胶体 | |
| D. | 水泥厂、冶金厂常用高压电除去烟尘,是因为烟尘粒子带电荷 |

| A. | ①② | B. | ③④ | C. | ②③ | D. | ②④ |
| 选项 | 学生甲 | 学生乙 |
| A | 向NaHCO3溶液中逐滴加入盐酸 | 向盐酸中逐滴加入NaHCO3溶液 |
| B | 向AlCl3溶液中滴加NaOH溶液 | 向NaOH溶液中滴加入AlCl3溶液 |
| C | 向FeCl2溶液中滴加KSCN溶液,再通入Cl2 | 向FeCl2溶液中通入Cl2,再滴加KSCN溶液 |
| D | 向Al2(SO4)3溶液中滴加氨水 | 向Al2(SO4)3溶液中滴加NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 推广“绿色自由”计划,吸收空气中的CO2并利用廉价能源合成汽油 | |
| B. | 做好空气质量预报工作,以便污染程度高时进行有效防护 | |
| C. | 工业废水的“再生”处理,用于道路保洁.城市喷泉和洗车等 | |
| D. | 利用风能.生物能发电,强制实施火力发电用煤的脱硫处理 |
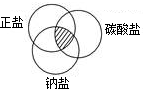 对于数以万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可代替的.现有碳、二氧化碳、氧化铁、澄清石灰水、稀硫酸和碳酸钠溶液等六种物质.通过常见分类法中的交叉分类法,可推出符合右上图阴影的物质的化学式是Na2CO3.
对于数以万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可代替的.现有碳、二氧化碳、氧化铁、澄清石灰水、稀硫酸和碳酸钠溶液等六种物质.通过常见分类法中的交叉分类法,可推出符合右上图阴影的物质的化学式是Na2CO3.