题目内容
标出下列氧化还原反应中电子转移方向和数目,并指出氧化剂,还原剂.
(1)2H2+O2
2H2O
(2)4P+5O2
2P2O5
(3)2KClO3
2KCl+3O2.
(1)2H2+O2
| ||
(2)4P+5O2
| ||
(3)2KClO3
| ||
| △ |
考点:氧化还原反应
专题:氧化还原反应专题
分析:(1)反应中H元素化合价升高,被氧化,O元素化合价降低被还原;
(2)反应中P元素化合价升高,被氧化,O元素化合价降低被还原;
(3)反应中Cl元素化合价降低,O元素化合价升高,以此解答该题.
(2)反应中P元素化合价升高,被氧化,O元素化合价降低被还原;
(3)反应中Cl元素化合价降低,O元素化合价升高,以此解答该题.
解答:
解:(1)反应中H元素化合价升高,被氧化,O元素化合价降低被还原,用双线桥表示其电子转移情况为: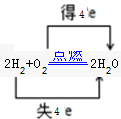 ,O2为氧化剂,H2为还原剂,
,O2为氧化剂,H2为还原剂,
答: ,O2为氧化剂,H2为还原剂;
,O2为氧化剂,H2为还原剂;
(2)反应中P元素化合价升高,被氧化,O元素化合价降低被还原,用双线桥表示其电子转移情况为: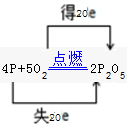 ,O2为氧化剂,P为还原剂,
,O2为氧化剂,P为还原剂,
答: ,O2为氧化剂,P为还原剂;
,O2为氧化剂,P为还原剂;
(3)反应中Cl元素化合价由+5价降低为KCl中-1价,氧元素由-2价升高为O2中0价,氧化剂和还原剂都是KClO3,转移电子数为12,用双线桥表示其电子转移情况为: ,
,
答: ;KClO3既是氧化剂也是还原剂.
;KClO3既是氧化剂也是还原剂.
 ,O2为氧化剂,H2为还原剂,
,O2为氧化剂,H2为还原剂,答:
 ,O2为氧化剂,H2为还原剂;
,O2为氧化剂,H2为还原剂;(2)反应中P元素化合价升高,被氧化,O元素化合价降低被还原,用双线桥表示其电子转移情况为:
 ,O2为氧化剂,P为还原剂,
,O2为氧化剂,P为还原剂,答:
 ,O2为氧化剂,P为还原剂;
,O2为氧化剂,P为还原剂;(3)反应中Cl元素化合价由+5价降低为KCl中-1价,氧元素由-2价升高为O2中0价,氧化剂和还原剂都是KClO3,转移电子数为12,用双线桥表示其电子转移情况为:
 ,
,答:
 ;KClO3既是氧化剂也是还原剂.
;KClO3既是氧化剂也是还原剂.
点评:本题考查氧化还原反应,为高频考点,侧重于基本概念、电子转移表示方法的考查,难度不大,注意对基础知识的理解掌握.

练习册系列答案
相关题目
CaC2是离子型金属碳化物,容易发生水解反应,生成乙炔和氢氧化钙.现有ZnC2、Al4C3、Mg2C3、Li2C2等,同属于离子型金属碳化物,也很容易发生水解反应.请从CaC2跟H2O反应生成C2H2的反应过程进行思考,从中得到必要的启示,判断下列物质的水解产物是C3H4的是( )
| A、ZnC2 |
| B、Al4C3 |
| C、Mg2C3 |
| D、Li2C2 |
下列垃圾中,不适合卫生填埋、焚烧、堆肥等处理方法的是( )
| A、厨余垃圾 | B、废电池 |
| C、植物秸秆 | D、织物垃圾 |
做过银镜反应的试管内壁有一层银,应该用下列物质中的哪种除去( )
| A、浓氨水 | B、盐酸 |
| C、稀硝酸 | D、烧碱液 |
科学家刚刚发现了某种元素的一个原子,其质量是ag,12C的一个原子质量是bg,NA是阿伏伽德罗常数的值,下列说法正确的是( )
| A、该原子的摩尔质量是:aNA | ||
B、Wg该原子的物质的量是:
| ||
C、Wg该原子中含有
| ||
D、由已知信息可得:NA=
|
将30mL0.5mol/LNaOH溶液加水稀释到500mL,稀释后溶液的浓度为( )
| A、0.1mol/L |
| B、0.3mol/L |
| C、0.05mol/L |
| D、0.03mol/L |