题目内容
在NO2与H2O的反应中( )
| A、H2O是还原剂 |
| B、氧化剂与还原剂的质量比为2:1 |
| C、HNO3是氧化剂 |
| D、生成 1mol HNO3时,转移电子1mol |
考点:氧化还原反应
专题:氧化还原反应专题
分析:在3NO2+H2O═2HNO3+NO的反应中,N元素化合价由+4价分别变化为+5价,+2价,根据化合价的变化判断物质在氧化还原反应中的性质.
解答:
解:方程式为3NO2+H2O═2HNO3+NO,
A.只有N元素化合价发生变化,水既不是氧化剂也不是还原剂,故A错误;
B.该反应中N元素的化合价由+4价变为+5价和+2价,所以生成硝酸的二氧化氮是还原剂,其计量数是2,生成NO的二氧化氮是氧化剂,其计量数是1,所以氧化剂和还原剂的物质的量、质量之比都是1:2,故B错误;
C.HNO3为氧化产物,故C错误;
D.生成 1mol HNO3时,N元素化合价由+4价升高到+5价,转移电子1mol,故D正确.
故选D.
A.只有N元素化合价发生变化,水既不是氧化剂也不是还原剂,故A错误;
B.该反应中N元素的化合价由+4价变为+5价和+2价,所以生成硝酸的二氧化氮是还原剂,其计量数是2,生成NO的二氧化氮是氧化剂,其计量数是1,所以氧化剂和还原剂的物质的量、质量之比都是1:2,故B错误;
C.HNO3为氧化产物,故C错误;
D.生成 1mol HNO3时,N元素化合价由+4价升高到+5价,转移电子1mol,故D正确.
故选D.
点评:本题考查氧化还原反应,明确元素化合价是解本题关键,注意该反应中化合价变化的元素只有N元素,为易错点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列离子反应方程式正确的是( )
| A、过量二氧化碳通入“水玻璃”中:CO2+SiO32-+H2O═CO32-+H2SiO3↓ |
| B、氨水滴入AlCl3溶液中:Al3++3OH-═Al(OH)3↓ |
| C、FeO溶于稀HCl中:O2-+2H+═H2O |
| D、Al2O3溶于NaOH溶液中:Al2O3+2OH-+3H2O═2[Al(OH)4]- |
“让节约成为一种校园时尚”是我校同学在升旗仪式上发出的倡议.下列各项措施中,既节约又环保的是( )
| A、药厂用自来水稀释生产中产生的废水 |
| B、回收废旧电池 |
| C、尽可能步行或骑自行车上学,或乘地铁或坐公交车上学,少坐私家车 |
| D、尽量多地使用化肥和农药以提高农作物产量 |
下列图示与对应的叙述不相符的是( )


| A、图1表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 |
| B、图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| C、图3表示0.1000mol?L-1 NaOH溶液滴定20.00mL 0.1000mol?L-1醋酸溶液得到的滴定曲线 |
| D、若将10mL 0.1mol/L CH3COOH溶液与20mL 0.1mol/L NaOH溶液混合,则溶液中离子浓度关系:c(OH-)═c(H+)+c(CH3COO-)+2c(CH3COOH) |
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、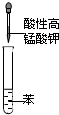 验证苯中是否有碳碳双键 |
B、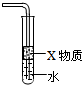 X若为苯,此装置可用于吸收氨气,防倒吸 |
C、 可除去HC1中含有的少量Cl2 |
D、 制备少量氧气 |
 由于锌的性质与铝相似,也易溶于强碱溶液放出氢气,因此可采用碱溶气体法测定镀锌铁皮锌镀层的厚度,装置如图.下列关于该实验的判断不正确的是( )
由于锌的性质与铝相似,也易溶于强碱溶液放出氢气,因此可采用碱溶气体法测定镀锌铁皮锌镀层的厚度,装置如图.下列关于该实验的判断不正确的是( )| A、发生的反应是:Zn+2NaOH→Na2ZnO2+H2↑ |
| B、反应结束冷却后,要用针筒抽气直至储液瓶中导管内外液面相平 |
| C、若镀锌铁皮的锌镀层中混有金属铝杂质,则会导致测定结果偏小 |
| D、碱溶气体法测定铁皮锌镀层厚度容易判断反应终点,却不及酸溶重量法简便 |
下列有关同分异构体数目的叙述中,错误的是( )
| A、甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种 |
| B、含有5个碳原子的饱和链烃,其一氯取代物共有8种 |
C、与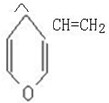 互为同分异构体的芳香族化合物有6种 互为同分异构体的芳香族化合物有6种 |
D、菲的结构简式为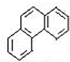 ,可有5种一硝基取代物 ,可有5种一硝基取代物 |
下列化合物中,苯环上的氢原子被溴原子取代,所得一溴代物有三种同分异构体的是( )

| A、①③ | B、①④ | C、②③ | D、③④ |
现有三组分散系:①CCl4和NaCl的混合液;②苯(沸点:80.1℃)和甲苯(沸点:110.6℃)的混合溶液(苯和甲苯是性质非常相似的一对互溶液体);③掺有碘化钾的碘水,分离以上各混合液的正确方法依次是( )
| A、分液、蒸馏、萃取 |
| B、萃取、蒸馏、分液 |
| C、蒸馏、萃取、分液 |
| D、分液、萃取、蒸馏 |