题目内容
根据表中信息,判断下列叙述中正确的是( )
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | Cl- | |
| ② | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| ③ | KClO3 | 浓盐酸 | / | Cl2 |
| A、表中①组反应可能有一种或两种元素被氧化 |
| B、氧化性强弱比较:KClO3>Cl2>Fe3+>Br2 |
| C、表中②组反应的离子方程式是2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O |
| D、表中③组反应的还原产物是KCl,电子转移数目是6e- |
考点:氧化还原反应
专题:氧化还原反应专题
分析:A.亚铁离子、溴离子均具有还原性,可被氯气氧化;
B.由①可知,亚铁离子先被氧化,则还原性亚铁离子大于溴离子;
C.电子不守恒;
D.反应为KClO3+6HCl=KCl+3Cl2↑+3H2O,氧化产物与还原产物均为Cl2.
B.由①可知,亚铁离子先被氧化,则还原性亚铁离子大于溴离子;
C.电子不守恒;
D.反应为KClO3+6HCl=KCl+3Cl2↑+3H2O,氧化产物与还原产物均为Cl2.
解答:
解:A.亚铁离子、溴离子均具有还原性,可被氯气氧化,少量氯气时只有亚铁离子被氧化,若氯气足量,亚铁离子、溴离子均被氧化,故A正确;
B.由①可知,亚铁离子先被氧化,则还原性亚铁离子大于溴离子,则氧化性为Br2>Fe3+,故B错误;
C.电子不守恒,正确的离子反应为2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O,故C错误;
D.反应为KClO3+6HCl=KCl+3Cl2↑+3H2O,氧化产物与还原产物均为Cl2,电子转移数目是5e-,故D错误;
故选A.
B.由①可知,亚铁离子先被氧化,则还原性亚铁离子大于溴离子,则氧化性为Br2>Fe3+,故B错误;
C.电子不守恒,正确的离子反应为2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O,故C错误;
D.反应为KClO3+6HCl=KCl+3Cl2↑+3H2O,氧化产物与还原产物均为Cl2,电子转移数目是5e-,故D错误;
故选A.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,注意氧化性的比较及优先氧化的规律,题目难度中等.

练习册系列答案
相关题目
下有三组混合物:①氯化钠和水;②硫酸钡和水;③煤油和水;④碘水的混合物.分离以上混合液的正确方法依次是( )
| A、分液、萃取、蒸馏、过滤 |
| B、蒸发、过滤、分液、萃取 |
| C、分液、蒸发、萃取、过滤 |
| D、蒸馏、萃取、分液、蒸发 |
在密闭容器中,可逆反应4CO+2NO2?4CO2+N2达到化学平衡时,下列说法正确的是( )
| A、反应混合气体的颜色不再变化 |
| B、CO、CO2两种物质浓度一定相等 |
| C、CO和NO2 全部变成CO2和N2 |
| D、单位时间若有4molCO消耗则同时有2molNO2生成 |
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、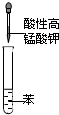 验证苯中是否有碳碳双键 |
B、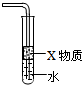 X若为苯,此装置可用于吸收氨气,防倒吸 |
C、 可除去HC1中含有的少量Cl2 |
D、 制备少量氧气 |
有氯气参加的化学反应一定不属于 ( )
| A、复分解反应 | B、置换反应 |
| C、取代反应 | D、加成反应 |
下列有关同分异构体数目的叙述中,错误的是( )
| A、甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种 |
| B、含有5个碳原子的饱和链烃,其一氯取代物共有8种 |
C、与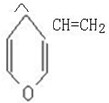 互为同分异构体的芳香族化合物有6种 互为同分异构体的芳香族化合物有6种 |
D、菲的结构简式为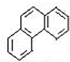 ,可有5种一硝基取代物 ,可有5种一硝基取代物 |
下列有关能量变化的说法中错误的是( )
| A、若反应物的总能量高于生成物的总能量,则该反应是吸热反应 |
| B、1mol石墨转化为金刚石,要吸收 1.895kJ的热能,则石墨比金刚石稳定 |
| C、化学变化中的能量变化主要由化学键的变化引起的 |
| D、化学变化必然伴随发生能量变化 |
含有非极性键的离子化合物是( )
| A、NaOH |
| B、Na2O2 |
| C、H2O2 |
| D、Cl2 |
可逆反应A(?)+a B(g)?C(g)+2D(g)(a为正整数).反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示.下列说法不正确的是( )


| A、当压强由p1变为 p2时,逆反应速率将变大 |
| B、该反应的正反应为放热反应 |
| C、若a=2,则A为液态或固体 |
| D、恒温恒容条件下,增加B的物质的量,B的转化率和该反应的化学平衡常数都将增大 |