题目内容
写出下列方程式
(1)惰性电极电解硫酸铜溶液:阳极: 阴极: 总反应:
(2)酸性条件下的甲烷燃料电池:负极: 正极:
(3)铁做阳极,碳做阴极电解饱和食盐水:阳极: 阴极: 总反应:
(4)银锌电池是一种高能电池,它质量轻、体积小,是人造卫星、宇宙火箭、空间电视转播站等的电源.电极材料为Zn 和Ag2O,电解质是KOH.总反应式:Zn+Ag2O=ZnO+2Ag,负极: 正极: .
(1)惰性电极电解硫酸铜溶液:阳极:
(2)酸性条件下的甲烷燃料电池:负极:
(3)铁做阳极,碳做阴极电解饱和食盐水:阳极:
(4)银锌电池是一种高能电池,它质量轻、体积小,是人造卫星、宇宙火箭、空间电视转播站等的电源.电极材料为Zn 和Ag2O,电解质是KOH.总反应式:Zn+Ag2O=ZnO+2Ag,负极:
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)惰性电极电解硫酸铜溶液,阳极氢氧根离子失电子,阴极铜离子得电子;
(2)酸性条件下的甲烷燃料电池,负极甲烷失电子,正极氧气得电子;
(3)铁做阳极,碳做阴极电解饱和食盐水,阳极Fe失电子,阴极氢离子得电子;
(4)银锌电池在负极锌失电子,正极氧化银得电子.
(2)酸性条件下的甲烷燃料电池,负极甲烷失电子,正极氧气得电子;
(3)铁做阳极,碳做阴极电解饱和食盐水,阳极Fe失电子,阴极氢离子得电子;
(4)银锌电池在负极锌失电子,正极氧化银得电子.
解答:
解:(1)惰性电极电解硫酸铜溶液,阳极氢氧根离子失电子生成氧气,则阳极的电极方程式为:4OH--4e-═H2O+O2↑,阴极铜离子得电子生成Cu,则阴极的电极方程式为:Cu2++2e-=Cu;总反应:2H2O+2CuSO4
2Cu+O2↑+2H2SO4 ;
故答案为:4OH--4e-═H2O+O2↑;Cu2++2e-=Cu;2H2O+2CuSO4
2Cu+O2↑+2H2SO4 ;
(2)酸性条件下的甲烷燃料电池,负极甲烷失电子生成二氧化碳和水,其负极的电极方程式为:CH4-8e-+2H2O═CO2+8H+,正极氧气得电子生成水,则正极的电极方程式为:O2+4H++4e-=2H2O;
故答案为:CH4-8e-+2H2O═CO2+8H+;O2+4H++4e-=2H2O;
(3)铁做阳极,碳做阴极电解饱和食盐水,阳极Fe失电子生成亚铁离子,则阳极的电极方程式为Fe-2e-=Fe2+,阴极氢离子得电子生成氢气,则阴极的电极方程式为:2H++2e-=H2↑;溶液中生成Fe2+、H2、和OH-,则电解的总方程式为:Fe+2H2O
Fe(OH)2↓+H2↑;
故答案为:Fe-2e-=Fe2+;2H++2e-=H2↑;Fe+2H2O
Fe(OH)2↓+H2↑;
(4)银锌电池中负极锌失电子,电极反应式:Zn+2OH--2e-=ZnO+H2O,正极氧化银得电子,则正极的电极方程式为Ag2O+H2O+2e-=2Ag+2OH-;
故答案为:Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-.
| ||
故答案为:4OH--4e-═H2O+O2↑;Cu2++2e-=Cu;2H2O+2CuSO4
| ||
(2)酸性条件下的甲烷燃料电池,负极甲烷失电子生成二氧化碳和水,其负极的电极方程式为:CH4-8e-+2H2O═CO2+8H+,正极氧气得电子生成水,则正极的电极方程式为:O2+4H++4e-=2H2O;
故答案为:CH4-8e-+2H2O═CO2+8H+;O2+4H++4e-=2H2O;
(3)铁做阳极,碳做阴极电解饱和食盐水,阳极Fe失电子生成亚铁离子,则阳极的电极方程式为Fe-2e-=Fe2+,阴极氢离子得电子生成氢气,则阴极的电极方程式为:2H++2e-=H2↑;溶液中生成Fe2+、H2、和OH-,则电解的总方程式为:Fe+2H2O
| ||
故答案为:Fe-2e-=Fe2+;2H++2e-=H2↑;Fe+2H2O
| ||
(4)银锌电池中负极锌失电子,电极反应式:Zn+2OH--2e-=ZnO+H2O,正极氧化银得电子,则正极的电极方程式为Ag2O+H2O+2e-=2Ag+2OH-;
故答案为:Zn+2OH--2e-=ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-.
点评:本题考查了原电池原理和电解池的原理,侧重于考查正负极电极反应式和阴阳极电极方程式的书写,题目难度中等,注意电解质溶液的酸碱性对电极方程式的影响.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
用下面的方案进行某些离子的检验,其中方案设计得最严密的是( )
A、检验试液中的SO42-:试液
| ||||
B、检验试液中的Fe2+:试液
| ||||
C、检验试液中的I-:试液
| ||||
D、检验试液中的CO32-:试液
|
下列说法正确的是( )
| A、室温下,将pH=2的醋酸与pH=12的NaOH溶液等体积混合,溶液显中性 |
| B、室温下,向pH=3的醋酸溶液加水稀释后,溶液中所有离子浓度均减小 |
| C、向含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 |
| D、向CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-) |
100ml 6mol/L H2SO4与过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
| A、Na2SO4(s) |
| B、NaOH |
| C、(NH4)2SO4(s)? |
| D、K2SO4溶液 |
以Al2(SO4)3溶液为原料之一,在实验室里制取少量Al(OH)3,并且易于分离,最好向溶液中加入( )
| A、NaOH 溶液 |
| B、氢氧化钡溶液 |
| C、氨水溶液 |
| D、澄清石灰水 |
下列各组离子一定能在指定环境中大量共存的是( )
| A、在c(HCO3-)=0.1mol/L的溶液中:Na+、AlO2-、Cl-、NO3- |
| B、在既能溶解Al(OH)3又能溶解H2SiO3的溶液中:Na+、NH4+、K+、NO3- |
| C、在水电离出的c(H+)=1×10-14mol/L的溶液中:Na+、SO42-、ClO-、Cl- |
| D、在pH=13的溶液中:SO32-、S2-、Na+、K+ |
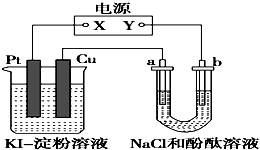 CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-═2CuI↓+I2而得到.如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI淀粉溶液中阳极周围变蓝色,则下列说法正确的是( )
CuI是一种不溶于水的白色固体,它可以由反应:2Cu2++4I-═2CuI↓+I2而得到.如图所示装置中,a、b都是惰性电极,通电一段时间后,在KI淀粉溶液中阳极周围变蓝色,则下列说法正确的是( )| A、若a极变红,则在Pt电极上:2I--2e-═I2,淀粉遇碘变蓝 |
| B、若b极变红,则在Pt电极上:4OH--4e-═2H2O+O2↑,O2将I-氧化为I2,淀粉遇碘变蓝 |
| C、若a极变红,则在Cu电极上:2Cu+4I--4e-═2CuI↓+I2,碘遇淀粉变蓝 |
| D、若b极变红,则在Cu极上:Cu-2e-═Cu2+,Cu2+显蓝色 |
已知下列两个反应中:4P(白磷,s)+5O2(g)=2P2O5(s)△H=-Q1 KJ/mol4P(红磷,s)+5O2(g)=2P2O5(s)△H=-Q2 KJ/mol且Q1>Q2,则( )
| A、燃烧白磷放出的能量比燃烧红磷放出的能量多 |
| B、白磷转化为红磷是属于放热反应 |
| C、白磷和红磷互为同素异形体 |
| D、等质量的白磷和红磷,白磷含有的能量比红磷的低 |
下列物质性质的比较中,正确的是( )
| A、原子半径:C>N>O |
| B、熔点:SiO2>CO2>H2O |
| C、热稳定性:NaHCO3>Na2CO3>H2CO3 |
| D、氧化性:Na+>Mg2+>Al3+ |