题目内容
某同学在探究废干电池内的黑色固体回收利用时,进行了如图所示实验:

请回答以下问题:
(1)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、泥三角、 ;
(2)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为 .
(3)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为 .
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
(5)根据以上的实验报告,关于滤液的成分,你的结论是: .
通过一定的操作从滤液中得到固体溶质,若要将所得固体溶质中的物质加以分离,可用 法.

请回答以下问题:
(1)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、泥三角、
(2)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为
(3)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
| 实验目的 | 操作 | 实验现象 | 结论 |
| 1.检验Cl- | 取少许滤液于试管中, | 含有Cl- | |
| 2.检验NH4+ | 取少许滤液于试管中, | 含有NH4+ | |
| 3.检验Zn2+ | 取少许滤液于试管中,加入 稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |
通过一定的操作从滤液中得到固体溶质,若要将所得固体溶质中的物质加以分离,可用
考点:物质分离和提纯的方法和基本操作综合应用,物质的检验和鉴别的实验方案设计,探究物质的组成或测量物质的含量
专题:实验设计题
分析:废旧干电池加水溶解,过滤后得到的残渣主要是二氧化锰、碳等,经灼烧后剩余固体为二氧化锰,加入双氧水中,可生成氧气,
(1)由图可知操作③是在坩埚内灼烧滤渣,通常把泥三角放在三角架上,再把坩埚放在泥三角上;
(2)能使双氧水迅速产生氧气的黑色物质是二氧化锰;
(3)使澄清石灰水变浑浊的气体有二氧化碳,二氧化碳可由黑色的碳单质灼烧制得;
(4)氯离子的检验是用硝酸酸化的硝酸银溶液,若产生白色沉淀,就证明含有氯离子;
铵根离子的检验是用浓氢氧化钠溶液并加热,然后用湿润的红色石蕊试纸检验,氨气能使湿润的红色石蕊试纸变蓝色;
(5)由实验可知滤液中含有氯化铵和氯化锌,分离所得的溶质固体,可以利用氯化铵的不稳定进行分离,采取加热法分离,再冷却收集氯化铵.
(1)由图可知操作③是在坩埚内灼烧滤渣,通常把泥三角放在三角架上,再把坩埚放在泥三角上;
(2)能使双氧水迅速产生氧气的黑色物质是二氧化锰;
(3)使澄清石灰水变浑浊的气体有二氧化碳,二氧化碳可由黑色的碳单质灼烧制得;
(4)氯离子的检验是用硝酸酸化的硝酸银溶液,若产生白色沉淀,就证明含有氯离子;
铵根离子的检验是用浓氢氧化钠溶液并加热,然后用湿润的红色石蕊试纸检验,氨气能使湿润的红色石蕊试纸变蓝色;
(5)由实验可知滤液中含有氯化铵和氯化锌,分离所得的溶质固体,可以利用氯化铵的不稳定进行分离,采取加热法分离,再冷却收集氯化铵.
解答:
解:废旧干电池加水溶解,过滤后得到的残渣主要是二氧化锰、碳等,经灼烧后剩余固体为二氧化锰,加入双氧水中,可生成氧气,
(1)对物质进行灼烧过程需要的仪器:酒精灯、玻璃棒、泥三角和三脚架、坩埚,故答案为:坩埚;
(2)能使带火星的木条复燃的气体是氧气,能使双氧水迅速产生氧气的黑色固体物质是二氧化锰,故答案为:二氧化锰(MnO2);
(3)灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,说明黑色固体生成二氧化碳气体,应为C(碳),故答案为:C(碳);
(4)氯离子的检验:取少许滤液于试管中,加入硝酸酸化的硝酸银溶液,银离子和氯离子反应生成不溶于水的白色沉淀氯化银;如果有白色沉淀生成,就说明有氯离子.
铵根离子的检验:铵根离子能和强碱在加热条件下反应生成氨气,氨气能使湿润的红色石蕊试纸变蓝色;如果湿润的红色石蕊试纸变蓝色,就说明有铵根离子存在.
故答案为:
(5)由实验可知滤液中含有氯化铵和氯化锌,分离所得的溶质固体,可以利用氯化铵的不稳定进行分离,采取加热法分离,再冷却收集氯化铵.
故答案为:滤液中含有氯化铵和氯化锌;加热.
(1)对物质进行灼烧过程需要的仪器:酒精灯、玻璃棒、泥三角和三脚架、坩埚,故答案为:坩埚;
(2)能使带火星的木条复燃的气体是氧气,能使双氧水迅速产生氧气的黑色固体物质是二氧化锰,故答案为:二氧化锰(MnO2);
(3)灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,说明黑色固体生成二氧化碳气体,应为C(碳),故答案为:C(碳);
(4)氯离子的检验:取少许滤液于试管中,加入硝酸酸化的硝酸银溶液,银离子和氯离子反应生成不溶于水的白色沉淀氯化银;如果有白色沉淀生成,就说明有氯离子.
铵根离子的检验:铵根离子能和强碱在加热条件下反应生成氨气,氨气能使湿润的红色石蕊试纸变蓝色;如果湿润的红色石蕊试纸变蓝色,就说明有铵根离子存在.
故答案为:
| 1.检验Cl- | 加入硝酸酸化的硝酸银溶液 | 有白色沉淀产生 | 含有Cl- |
| 2.检验NH4+ | 加入浓氢氧化钠溶液并加热,将润湿的红色石蕊试纸置于试管口附近 | 石蕊试纸变蓝色 | 含有NH4+ |
故答案为:滤液中含有氯化铵和氯化锌;加热.
点评:本题以对干电池物质成分的探究为载体,考查基本实验操作、离子的检验等,为高考常见题型,侧重于学生的分析能力和实验能力的考查,难度不大,熟悉中学阶段常见阴阳离子的检验方法,掌握实验基本操作.

练习册系列答案
相关题目
进行化学实验必须注意安全,下列说法不正确的是( )
| A、不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
| B、不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液 |
| C、从煤油中取用金属钠必需用镊子,不能用手触摸 |
| D、配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
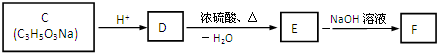
目前国家仍允许在面粉中添加过氧化苯甲酰来使面粉增白,但它的安全性已引起公众质疑.已知过氧化苯甲酰能发生如下反应:
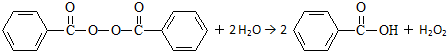
下列叙述不正确的是( )
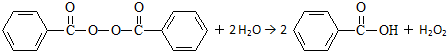
下列叙述不正确的是( )
| A、并非在食品中添加化学物质都对人体有害 |
| B、过氧化苯甲酰能使面粉增白的原因是它与水反应生成的H2O2具有漂白性 |
| C、苯甲酸的同分异构体中,既属于醛又属于酚的物质有4种 |
| D、甲苯经两步取代反应和两步催化氧化反应可转化为苯甲酸 |



 茶是我国人民喜爱的饮品,其中含有多种有益于人体健康的成分,据测定茶叶中含有450种以上的有机成分与15种以上的元素.某化学研究小组欲探究茶叶中钙元素的含量,设计了探究实验方案如下:(已知茶叶中的铝、铁元素对钙离子的测定有影响)
茶是我国人民喜爱的饮品,其中含有多种有益于人体健康的成分,据测定茶叶中含有450种以上的有机成分与15种以上的元素.某化学研究小组欲探究茶叶中钙元素的含量,设计了探究实验方案如下:(已知茶叶中的铝、铁元素对钙离子的测定有影响) 如图所示,当线路接通时,发现M(用紫色石磊试液浸过的滤纸)a端显蓝色,b端显红色,且知甲中电极材料是锌-银,乙中电极材料是铂-铜 且乙中两极不发生变化,回答:
如图所示,当线路接通时,发现M(用紫色石磊试液浸过的滤纸)a端显蓝色,b端显红色,且知甲中电极材料是锌-银,乙中电极材料是铂-铜 且乙中两极不发生变化,回答: