题目内容
20.由乙烯推测丙烯的结构或性质,正确的是( )| A. | 分子中3个碳原子在同一直线上 | |
| B. | 分子中所有原子都在同一平面上 | |
| C. | 分子中共价键的夹角为120° | |
| D. | 分子中共价键数为8,其中有一个碳碳双键 |
分析 乙烯是平面型结构,键角是120°,丙烯分子中也含有碳碳双键,所以丙烯分子中的3个碳原子在同一个平面内,但不在同一直线上;由于含有甲基,所以分子中所有原子不可能在同一平面,据此进行解答.
解答 解:A.丙烯分子中的3个碳原子在同一个平面内,但不在同一直线上,故A错误;
B.丙烯分子中含有甲基,所以分子中所有原子不可能在同一平面上,故B错误;
C.丙烯中甲基为立体结构,甲基中的碳氢键的夹角不是120°,故C错误;
D.丙烯分子中含有1个碳碳单键、1个碳碳双键和6个碳氢键,总共含有8个共价键,故D正确;
故选D.
点评 本题考查了有机物结构与性质,题目难度不大,明确乙烯、甲烷的结构为解答关键,注意熟练掌握常见有机物结构与性质,试题培养了学生的分析能力及知识迁移能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.2015年12月23日,北京的空气质量拉响警报,全市污染指数超过400,达到重度污染,严重影响人们的身体健康.关于空气污染,越来越需要引起我们的重视.下列说法正确的是( )
| A. | 二氧化硫、二氧化氮、一氧化碳和二氧化碳是空气质量报告中涉及的主要污染物 | |
| B. | 正常雨水的pH等于7 | |
| C. | 二氧化硫和二氧化氮是引起酸雨的主要气体 | |
| D. | 家用汽车有利于人们出行,需要大力推广应用 |
11.X、Y、Z为短周期主族元素,X的最外层电子数为内层电子数的2倍,Y的最高化合价与最低化合价的代数和为4,Z与Y同周期,Z的原子半径小于Y.下列叙述不正确的是( )
| A. | Z的氢化物是同主族简单氢化物中最稳定的 | |
| B. | 非金属性:Z>Y>X | |
| C. | XY2中各原子最外层均满足8电子结构 | |
| D. | X、Y的最高价氧化物对应的水化物酸性后者强 |
8.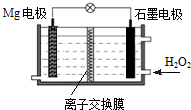 Mg-H2O2电池可用于无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如图.下列说法正确的是( )
Mg-H2O2电池可用于无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如图.下列说法正确的是( )
 Mg-H2O2电池可用于无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如图.下列说法正确的是( )
Mg-H2O2电池可用于无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如图.下列说法正确的是( )| A. | Mg电极是该电池的正极 | B. | H2O2在石墨电极上发生氧化反应 | ||
| C. | 该电池的总反应为:Mg+H2O2═Mg(OH)2 | D. | 溶液中Cl-向正极移动 |
15.科学上规定,1.01×105Pa、25℃时,拆开1mol气态AB分子,使之变为1mol气态A原子和气态B原子,所需要吸收的能量,叫A-B键的“键能”.根据物质的结构与化学键的键能值,可以粗略判断化学反应过程的热效应,下面是一些常见化学键的键能值.
(1)根据上表的数据,计算由Cl2(g)和H2(g)化合生成1molHCl(g)时所释放的能量.
(2)判断甲烷的氯代反应Cl2(g)+CH4(g)═CH3Cl(g)+HCl(g),是吸热反应还是放热反应?
| 化学键 | H-Cl | Cl-Cl | H-H | C-H | C-Cl |
| 键能/(kJ•mol-1) | 431.4 | 242.1 | 435.9 | 413.0 | 338.9 |
(2)判断甲烷的氯代反应Cl2(g)+CH4(g)═CH3Cl(g)+HCl(g),是吸热反应还是放热反应?
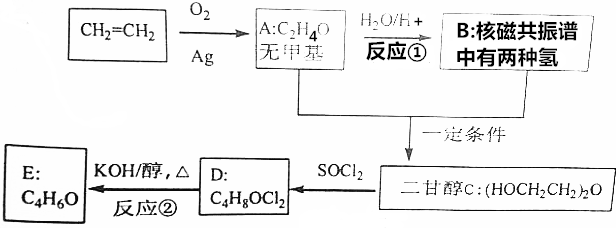
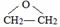 DClCH2CH2OCH2CH2Cl;
DClCH2CH2OCH2CH2Cl;