题目内容
15.科学上规定,1.01×105Pa、25℃时,拆开1mol气态AB分子,使之变为1mol气态A原子和气态B原子,所需要吸收的能量,叫A-B键的“键能”.根据物质的结构与化学键的键能值,可以粗略判断化学反应过程的热效应,下面是一些常见化学键的键能值.| 化学键 | H-Cl | Cl-Cl | H-H | C-H | C-Cl |
| 键能/(kJ•mol-1) | 431.4 | 242.1 | 435.9 | 413.0 | 338.9 |
(2)判断甲烷的氯代反应Cl2(g)+CH4(g)═CH3Cl(g)+HCl(g),是吸热反应还是放热反应?
分析 化学反应中旧键断裂需要吸收能量,新键形成需要放出能量,化学反应中的反应热△H=反应物总键能-生成物总键能,据此结合Cl2+H2=2HCl,Cl2(g)+CH4(g)═CH3Cl(g)+HCl(g)以及表中键能值解答,△H>0吸热,反之放热.
解答 解:(1)Cl2+H2=2HCl,△H=反应物的键能和-生成物的键能和=242.1 KJ/mmol+435.9KJ/mol-2×431.4KJ/mol=-184.8KJ/mol,△H<0反应放热,生成1molHCl时放热184.8×$\frac{1}{2}$KJ=92.4KJ,
答:由Cl2(g)和H2(g)化合生成1molHCl(g)时所释放的能量为92.4KJ;
(2)1molCH4中含有4molC-H键,反应CH4(g)+Cl2(g)=CH3Cl(g)+HCl(g);△H=-106kJ/mol,反应焓变△H=4×[C-H]+[Cl-Cl]-[(C-Cl)+3×(C-H)+(H-Cl)]=4×[413.0]+[242.1]-[(338.9 )+3×(413.0 )+(431.4)]KJ/mol=-115.2KJ/mol,△H<0该反应放热,
答:甲烷的氯代反应Cl2(g)+CH4(g)═CH3Cl(g)+HCl(g),是放热反应.
点评 本题考查反应热与化学键的关系,要正确利用利用△H=反应物的键能和-生成物的键能和,注意△H与化学计量数的对应,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.实验室用锌粒与2mol/L的硫酸制取氢气,下列措施不能增大该反应速率的是( )
| A. | 加水稀释 | B. | 适当增大硫酸浓度 | ||
| C. | 加热 | D. | 用锌粉代替锌粒 |
6.对下列各组实验所作的解释正确的是( )
| 选项 | 实验操作 | 现象 | 解释 |
| A | 向AlCl3溶液中逐滴加入NaOH溶液并振荡 | 产生白色沉淀,后沉淀逐渐溶解 | 铝元素具有一定的非金属性 |
| B | 将Fe(NO3)2固体溶于稀硫酸,滴加KSCN溶液 | 溶液变红 | 稀硫酸将Fe2+氧化为Fe3+ |
| C | 向KBrO3溶液中加入少量CCl4,然后通入少量Cl2,充分振荡,静置 | 下层呈橙色 | 氧化性:Cl2>Br2 |
| D | 将充有NO2的玻璃球放入热水中 | 红棕色加深 | 2NO2?N2O4△H>0 |
| A. | A | B. | B | C. | C | D. | D |
10.T℃时,在甲、乙、丙三个容积均为2L的恒容密闭容器中投入SO2(g)和O2(g),发生反应:2SO2(g)+O2(g)?2SO3(g),5min时甲达到平衡.其起始量及SO2的平衡转化率如表所示.下列叙述不正确的是( )
| 容器 | 甲 | 乙 | 丙 | |
| 起始量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | |
| SO2的平衡转化率 | 80% | α1 | α2 | |
| A. | 0~5min内,甲中SO2的反应速率为0.032mol•L-1•min-1 | |
| B. | T℃时,该反应的平衡常数K=400 | |
| C. | 平衡时,SO2的转化率:α1<80%<α2 | |
| D. | 平衡时,丙中气体平均相对分子质量与甲相同 |
20.由乙烯推测丙烯的结构或性质,正确的是( )
| A. | 分子中3个碳原子在同一直线上 | |
| B. | 分子中所有原子都在同一平面上 | |
| C. | 分子中共价键的夹角为120° | |
| D. | 分子中共价键数为8,其中有一个碳碳双键 |
7.化学科学、技术、社会、环境密切相关.下列说法不正确的是( )
| A. | 利用蓝绿藻等低等生物和微生物在阳光作用下使水分解产生氢气,该方法符合绿色化学原则 | |
| B. | 12C、13C和14C互为同位素,它们的放射性可用于考古断代,可测定生物体死亡的年代 | |
| C. | 食品脱氧剂(含铁粉、氯化钠、炭粉等)的脱氧原理与钢铁的吸氧腐蚀相同 | |
| D. | 利用生物方法脱除生活污水中的氮和磷,防止水体富营养化 |
16.已知Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O.甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响.设计实验如表(所取溶液体积均为10mL):
其他条件不变时:探究温度对化学反应速率的影响,应选择①⑤或②④(填实验编号);
探究浓度对化学反应速率的影响,应选择①②或①③或④⑤(填实验编号);
若同时选择①②③溶液变浑浊的时间,探究比较改变不同反应物浓度对反应速率的影响对化学反应速率的影响.
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol•L-1 | c(H2SO4)/mol•L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.2 | 0.1 |
| ③ | 25 | 0.1 | 0.2 |
| ④ | 50 | 0.2 | 0.1 |
| ⑤ | 50 | 0.1 | 0.1 |
探究浓度对化学反应速率的影响,应选择①②或①③或④⑤(填实验编号);
若同时选择①②③溶液变浑浊的时间,探究比较改变不同反应物浓度对反应速率的影响对化学反应速率的影响.
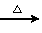 CO2↑+2H2O↑+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g。将反应后气体通入2L0.lmol/L的澄清Ca(OH)2溶液,充分吸收,生成沉淀10g。求:
CO2↑+2H2O↑+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻了4.8g。将反应后气体通入2L0.lmol/L的澄清Ca(OH)2溶液,充分吸收,生成沉淀10g。求: