题目内容
NO是大气污染物之一,但少量的NO在人体内具有扩张血管、增强记忆的功能.通常状况下,NO密度比空气略大,极易与氧气反应,难溶于水.实验室收集NO的装置是( )
A、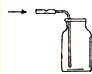 |
B、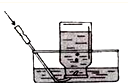 |
C、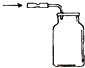 |
D、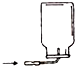 |
考点:氮的氧化物的性质及其对环境的影响,气体的收集
专题:氮族元素
分析:收集气体有两种方法:排水法和排空气法,排水法适合于难溶于水且不和水反应的气体;排空气法有向上排空气法和向下排空气法两种,向上排空气法适合于密度比空气大而且不与空气成分发生反应的气体,向下排空气法适合于密度比空气小而且不与空气成分发生反应的气体.
解答:
解:NO难溶于水,可用排水法收集;密度比空气的略大且极易和空气中的氧气反应,故不能用排空气法收集;
故选B.
故选B.
点评:本题考查了气体收集方法分析,一氧化氮性质应用,排水法收集的气体较为纯净,是较为理想的收集方法,一般有毒气体不适合用排空气的方法,题目较简单.

练习册系列答案
相关题目
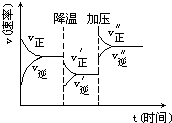 图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )
图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断( )| A、正反应是吸热反应 |
| B、若A、B是气体,则D是液体或固体 |
| C、加压反应向逆方向进行 |
| D、A、B、C、D均为气体 |
常温条件下,一密闭容器中以1:2:3的比例充入NO、N2、NO2,在条件不变的情况下,向容器中充入与NO2等体积的O2,充分反应后,有关容器中的气体的下列叙述中正确的是(不考虑NO2转化为N2O4)( )
| A、NO、N2、NO2、O2的体积比为1:2:3:3 |
| B、N2、NO2、O2的体积比为2:3:2 |
| C、NO、NO2、O2的体积比为4:3:1 |
| D、N2、NO2、O2的体积比为4:8:5 |
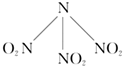 科学家最近研制出可望成为高效火箭推进剂N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法不正确的是( )
科学家最近研制出可望成为高效火箭推进剂N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法不正确的是( )| A、分子中的化学键有极性键和非极性键 |
| B、分子中四个氮原子位于正四面体的顶点 |
| C、该物质的熔、沸点可能比NH3高 |
| D、15.2g该物质含有6.02×1023个原子 |
如果你家里的食用花生油混有水份,你将采用下列何种方法分离( )
a.过滤 b.蒸馏c.分液 d.萃取.
a.过滤 b.蒸馏c.分液 d.萃取.
| A、a | B、b | C、c | D、d |
下列有关氯气的叙述中正确的是( )
| A、氯气在常温下能与铁反应,故不能用铁罐存放液氯 |
| B、液氯和氯水不是同一物质 |
| C、点燃氢气和氯气的混合气体可以制取氯化氢 |
| D、用氯气对生活用水进行消毒的原因是氯气能杀灭细菌 |
标准状况下,将4.48L的NO2和NO组成的混合气体通入100mL的水中,气体体积缩小为2.24L,假设溶液的体积不变,则下列说法中错误的是( )
| A、所得溶液中溶质的物质的量浓度为1.0mol?L-1 |
| B、剩余气体中氮元素与氧元素的质量为8:7 |
| C、原混合气体中NO2和NO的体积比为1:1 |
| D、反应过程中转移的电子总数为0.1mol |
一定不是同分异构体的一组物质是( )
| A、含相同碳原子数的饱和醛和酮 |
| B、含相同碳原子数的饱和一元羧酸与酯 |
| C、乙醇与乙醚 |
| D、对甲苯酚与苯甲醇 |
已知碱能除去硝酸工业废气中的NO2和NO:NO2+NO+2NaOH═2NaNO2+H2O;2NO2+2NaOH═NaNO2+NaNO3+H2O.根据上述反应原理,下列气体中不能被过量的NaOH吸收的是( )
| A、1mol O2和4mol NO2 |
| B、1mol NO和4mol NO2 |
| C、1mol O2和4mol NO |
| D、1mol NO2和4mol NO |