题目内容
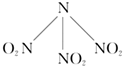 科学家最近研制出可望成为高效火箭推进剂N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法不正确的是( )
科学家最近研制出可望成为高效火箭推进剂N(NO2)3(如图所示).已知该分子中N-N-N键角都是108.1°,下列有关N(NO2)3的说法不正确的是( )| A、分子中的化学键有极性键和非极性键 |
| B、分子中四个氮原子位于正四面体的顶点 |
| C、该物质的熔、沸点可能比NH3高 |
| D、15.2g该物质含有6.02×1023个原子 |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:A、同种元素间形成非极性键,不同非金属元素间形成极性键;
B、该分子不是正四面体形;
C、该分子的相对分子质量较大,沸点比氨气的高;
D、根据质量求出分子的物质的量,再求原子个数.
B、该分子不是正四面体形;
C、该分子的相对分子质量较大,沸点比氨气的高;
D、根据质量求出分子的物质的量,再求原子个数.
解答:
解:A、同种元素间形成非极性键,不同非金属元素间形成极性键,N与N之间形成非极性键,N与O之间形成极性键,故A正确;
B、由图可知该分子上顶点与三个下顶点所含原子不同,不是正四面体形,故B错误;
C、N(NO2)3分子的相对分子质量较大,沸点比氨气的高,故C正确;
D、N(NO2)3的相对分子质量为152,15.2 g N(NO2)3为0.1mol,该物质的分子中所含原子为1mol,即6.02×1023个原子,故D正确.
故选B.
B、由图可知该分子上顶点与三个下顶点所含原子不同,不是正四面体形,故B错误;
C、N(NO2)3分子的相对分子质量较大,沸点比氨气的高,故C正确;
D、N(NO2)3的相对分子质量为152,15.2 g N(NO2)3为0.1mol,该物质的分子中所含原子为1mol,即6.02×1023个原子,故D正确.
故选B.
点评:本题为通过给出信息,考查了物质的结构和性质,题目难度中等,熟悉氨气分子的模型是解题的关键,注意知识的迁移应用.

练习册系列答案
相关题目
有效碰撞是指( )
| A、活化分子之间的碰撞 |
| B、分子间的碰撞 |
| C、反应物分子发生合适取向的碰撞 |
| D、活化分子之间发生合适取向的碰撞 |
下列对阿伏加德罗常数的叙述中,正确的是( )
| A、阿伏加德罗常数就是6.02×1024 mol-1 |
| B、阿伏加德罗常数为2mol指定粒子的粒子数 |
| C、阿伏加德罗常数为12 g碳所含的碳原子数 |
| D、阿伏加德罗常数用符号NA表示,其值约为6.02×1023 mol-1 |
向20mL1mol/LH2SO4溶液中加入2OmL1mol/LNaOH溶液,充分反应,下列 说法正确的是( )
| A、溶液中c(OH-)═c(H+),溶液呈中性 |
| B、c(Na+)═c(SO42-)═c(H+) |
| C、H2SO4剩余,溶液呈酸性 |
| D、溶液的导电能力和原H2SO4溶液相同 |
在0.1mol?L-1的NaHCO3溶液中,下列关系式正确的是( )
| A、c(Na+)>c(HCO3-)>c(H+)>c(OH-) |
| B、c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-) |
| C、c(Na+)=c(HCO3-)>c(OH-)>c(H+) |
| D、c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-) |
下列分子中,不含手性碳原子的是( )
A、 |
B、 |
C、 |
| D、CH3CHClCH2CHO |
工业生产上常使用催化剂,因为它可以( )
| A、提高反应进行的程度 |
| B、使平衡向正反应方向移动 |
| C、是生成物更纯净 |
| D、使容器中气体的密度不再发生变化 |