题目内容
11. 铜版画的一种制版方法.以沥青涂于薄铜板表面作防腐膜,用刀刻去防腐膜作画,然后放在FeCl3腐蚀液中.刮去膜之处被腐蚀,形成凹线.印刷时凹线可储油墨,在铜版机纸压制下油墨吸于纸上,形成典雅、庄重的铜版画.
铜版画的一种制版方法.以沥青涂于薄铜板表面作防腐膜,用刀刻去防腐膜作画,然后放在FeCl3腐蚀液中.刮去膜之处被腐蚀,形成凹线.印刷时凹线可储油墨,在铜版机纸压制下油墨吸于纸上,形成典雅、庄重的铜版画.(1)写出FeCl3腐蚀铜板的离子方程式2Fe3++Cu=2Fe2++Cu2+;
(2)下列措施可以加快铜板的腐蚀速率的有AC(填编号);
A.加热B.加氯化铜C.加少量碳粉D.加盐酸
(3)通常不采用加快腐蚀速率的原因是反应速率过快不易控制凹线的质量,从而影响版画的质量;
(4)除去沥青防腐膜后版即形成.可用B除去防腐膜(填编号);
A.饱和Na2CO3溶液B.煤油C.酸液D.碱液
(5)实验室用固体氯化铁配置FeCl3溶液的简单操作是将固体氯化铁溶于浓盐酸中,再加水稀释;
(6)腐蚀后的废液(酸性)中加入NaNO3,产生NO气体,写出发生反应的离子方程式,并注明电子转移的方向和数目:
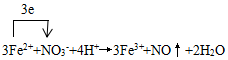 ;
;(7)要验证腐蚀后的废液中含有Fe3+,可在溶液中加入试剂KSCN溶液,现象溶液呈红色.
分析 (1)Fe3+有强氧化性,能把金属铜氧化成铜离子;
(2)加热或形成原电池能加快反应速率;
(3)反应速率太快时,溶解的铜较多;
(4)沥青易溶于有机溶剂;
(5)FeCl3易水解应该加酸抑制水解;
(6)亚铁离子与硝酸反应生成铁离子和NO;
(7)检验三价铁离子用硫氰化钾溶液.
解答 解:(1)Fe3+有强氧化性,能把金属铜氧化成铜离子,自身被还原成 Fe2+,反应方程式为2Fe3++Cu=2Fe2++Cu2+,
故答案为:2Fe3++Cu=2Fe2++Cu2+;
(2)加热能加快化学反应速率,向溶液中加碳粉,碳、Cu、氯化铁溶液三者形成原电池,Cu作负极能加快腐蚀铜的反应速率;
故答案为:AC;
(3)反应速率太快时,溶解的铜较多,不易控制凹线的质量,从而影响版画的质量;
故答案为:反应速率过快不易控制凹线的质量,从而影响版画的质量;
(4)沥青是有机物易溶于有机溶剂,所以选择煤油作溶剂可以除去防腐膜;
故答案为:B;
(5)FeCl3易水解,固体氯化铁配置FeCl3溶液时,将固体氯化铁溶于浓盐酸中,再加水稀释,可以抑制氯化铁的水解;
故答案为:将固体氯化铁溶于浓盐酸中,再加水稀释;
(6)亚铁离子与硝酸反应生成铁离子和NO,反应中Fe元素化合价升高1价,N元素的化合价降低3价,转移的电子数为3,则电子转移的方向和数目为: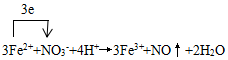 ;
;
故答案为: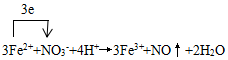 ;
;
(7)检验三价铁离子用硫氰化钾溶液,三价铁离子与硫氰化钾溶液反应会生成红色的溶液;
故答案为:KSCN溶液;溶液呈红色.
点评 本题考查了Cu、Fe以及其化合物的性质、离子检验、氧化还原反应,题目难度中等,侧重于考查学生对基础知识的综合应用能力,注意把握常见离子的检验方法以及氧化还原反应中电子转移的表示方法.

练习册系列答案
相关题目
19.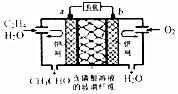 中石化于2012年将年产120万吨的乙烯工程落户大庆,乙烯是有机化工工业的重要原料,有很多重要用途.如:乙烯催化氧化成乙醛可设计成如下图所示的燃料电池,在制备乙醛的同时还可获得电能,其总反应化学方程式为:2CH2═CH2+O2→2CH3CHO.下列有关说法正确的是( )
中石化于2012年将年产120万吨的乙烯工程落户大庆,乙烯是有机化工工业的重要原料,有很多重要用途.如:乙烯催化氧化成乙醛可设计成如下图所示的燃料电池,在制备乙醛的同时还可获得电能,其总反应化学方程式为:2CH2═CH2+O2→2CH3CHO.下列有关说法正确的是( )
 中石化于2012年将年产120万吨的乙烯工程落户大庆,乙烯是有机化工工业的重要原料,有很多重要用途.如:乙烯催化氧化成乙醛可设计成如下图所示的燃料电池,在制备乙醛的同时还可获得电能,其总反应化学方程式为:2CH2═CH2+O2→2CH3CHO.下列有关说法正确的是( )
中石化于2012年将年产120万吨的乙烯工程落户大庆,乙烯是有机化工工业的重要原料,有很多重要用途.如:乙烯催化氧化成乙醛可设计成如下图所示的燃料电池,在制备乙醛的同时还可获得电能,其总反应化学方程式为:2CH2═CH2+O2→2CH3CHO.下列有关说法正确的是( )| A. | 该电池电极a为正极,b为负极 | |
| B. | 电子移动方向:电极a→磷酸溶液→电极b | |
| C. | 负极反应式为:CH2═CH2-2e-+H2O═CH3CHO+2H+ | |
| D. | b电极有2.24LO2反应,溶液中有0.4molH+迁移到b电极上反应 |
6.下列各组物质的熔沸点能用化学键的强弱解释的是( )
| A. | H2O>H2S | B. | NaCl>O2 | C. | Na>K | D. | SiO2>CO2 |
16.为了检验某固体物质中是否含有NH4+,一定用不到的试剂或试纸是( )
| A. | NaOH溶液 | B. | 浓盐酸 | C. | 稀硫酸 | D. | 红色石蕊试纸 |
20.下列过程对应的离子方程式正确的是( )
| A. | NaHSO3溶于水呈酸性:NaHSO3═Na++H++SO32- | |
| B. | 在Na2S2O3溶液中滴加稀硫酸:2H++S2O32-═SO2↑+S↓+H2O | |
| C. | 浓盐酸与MnO2反应制氯气:MnO2+4HCl═Mn2++2Cl2+2H2O | |
| D. | 工业冶炼Mg:2Mg2++2O2-$\frac{\underline{\;电解\;}}{\;}$2Mg+O2↑ |
6. 肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题:
肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题:
(1)N2H4中N原子核外最外层达到8电子稳定结构.写出N2H4的结构式: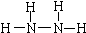 .
.
(2)实验室用两种固体制取NH3的反应化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
(3)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为2NH3+NaClO=N2H4+NaCl+H2O.
(4)肼一空气燃料电池是一种碱性环保电池,该电池放电时,负极的反应式为N2H4+4OH--4e-=N2+4H2O.
(5)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2]反应的化学方程式为2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(l),该反应的平衡常数和温度关系如表:
①焓变△H<0(填“>”、“<”或“=”).
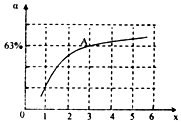
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)[n(NH3):n(CO2]=x,如图是氨碳比(x)与CO2平衡转化率(α)的关系.α随着x增大而增大的原因是c(NH3)增大,平衡正向移动.图中A点处,NH3的平衡转化率为42%.
(6)在恒温恒容密闭容器中按照甲、乙、丙三种方式分别投料,发生反应:N2(g)+3H2(g)?2NH3(g),测得甲容器中H2的平衡转化率为40%.
①判断乙容器中反应进行的方向是逆向(填“正向或“逆向”)移动.
②达平衡时,甲、乙、丙三容器中NH3的体积分数大小顺序为丙>甲=乙.
(7)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式:4NH3+5O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O,科学家利用此原理,设计成氨气一氧气燃料电池,则通入氨气的电极是负极 (填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为2NH3-6e-+6OH-=N2+6H2O.
(8)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g).在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是c(填字母代号).
a.增大压强 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
(9)如果某氨水的电离程度为1%,浓度为0.01mol/LMgCl2溶液滴加氨水至开始产生沉淀时(不考虑溶液体积变化),溶液中的NH3•H2O的浓度为0.002mol/L[已知Ksp[Mg(OH)2]=4.0×10-12].
 肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题:
肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题:(1)N2H4中N原子核外最外层达到8电子稳定结构.写出N2H4的结构式:
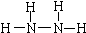 .
.(2)实验室用两种固体制取NH3的反应化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
(3)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为2NH3+NaClO=N2H4+NaCl+H2O.
(4)肼一空气燃料电池是一种碱性环保电池,该电池放电时,负极的反应式为N2H4+4OH--4e-=N2+4H2O.
(5)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2]反应的化学方程式为2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(l),该反应的平衡常数和温度关系如表:
| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)[n(NH3):n(CO2]=x,如图是氨碳比(x)与CO2平衡转化率(α)的关系.α随着x增大而增大的原因是c(NH3)增大,平衡正向移动.图中A点处,NH3的平衡转化率为42%.
| n(N2) | n(H2) | n(NH3) | |
| 甲 | 1mol | 3mol | 0mol |
| 乙 | 0.5mol | 1.5mol | 1mol |
| 丙 | 0mol | 0mol | 4mol |
①判断乙容器中反应进行的方向是逆向(填“正向或“逆向”)移动.
②达平衡时,甲、乙、丙三容器中NH3的体积分数大小顺序为丙>甲=乙.
(7)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式:4NH3+5O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O,科学家利用此原理,设计成氨气一氧气燃料电池,则通入氨气的电极是负极 (填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为2NH3-6e-+6OH-=N2+6H2O.
(8)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g).在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是c(填字母代号).
a.增大压强 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
(9)如果某氨水的电离程度为1%,浓度为0.01mol/LMgCl2溶液滴加氨水至开始产生沉淀时(不考虑溶液体积变化),溶液中的NH3•H2O的浓度为0.002mol/L[已知Ksp[Mg(OH)2]=4.0×10-12].
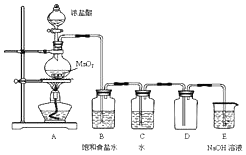 某化学兴趣小组制备饱和氯水并对饱和氯水与碳酸钙的反应进行研究.
某化学兴趣小组制备饱和氯水并对饱和氯水与碳酸钙的反应进行研究.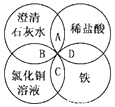 铁、稀硫酸、Ba(OH)2溶液、CuSO4溶液是中学化学常见的物质,这四种物质间的反应关系如图所示,图中两圆相交部分(A、B、C、D)表示物质之间可能发生的反应,请回答下列问题:
铁、稀硫酸、Ba(OH)2溶液、CuSO4溶液是中学化学常见的物质,这四种物质间的反应关系如图所示,图中两圆相交部分(A、B、C、D)表示物质之间可能发生的反应,请回答下列问题: