题目内容
4.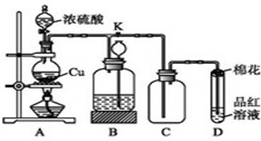 某化学兴趣小组为探究铜与浓硫酸的反应,用下图所示装置进行有关实验. 甲同学取ag Cu 片和12ml 18mol/L浓H2SO4放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的H2SO4和Cu剩余.
某化学兴趣小组为探究铜与浓硫酸的反应,用下图所示装置进行有关实验. 甲同学取ag Cu 片和12ml 18mol/L浓H2SO4放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的H2SO4和Cu剩余.(1)Cu与浓H2SO4反应的化学方程式是Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑.
(2)装置D盛有品红溶液,当C中气体集满后,D中有可能观察到的现象是品红溶液褪色,
(3)装置D中试管口放置的棉花中应浸一种液体,这种液体是氢氧化钠溶液,其作用是在试管口吸收二氧化硫.
(4)装置B的作用是贮存多余的气体.当D处有明显现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中试剂瓶中液面下降,长颈漏斗中液面上升.B中应放置的液体是d(填序号).
a.饱和Na2SO3溶液 b.酸性 KMnO4溶液 c.浓溴水 d.饱和NaHSO3溶液
(5)反应完毕后,烧瓶中还有一定量的余酸,为什么却不能使Cu完全溶解的原因是随着反应进行,硫酸被消耗,产物有水生成,所以浓硫酸变成稀硫酸,反应会停止.使用足量的下列药品不能用来证明反应结束后的烧瓶中的确有余酸的是b(填序号).
a.Fe粉 b.BaCl2溶液 c.CuO d.Na2CO3溶液
(6)实验中某学生向A中反应后溶液中通入一种常见气体单质,使铜片全部溶解且仅生成硫酸铜溶液,请问该气体单质是O2,该反应的化学方程式是2Cu+O2+2H2SO4═2CuSO4+2H2O.
分析 探究铜与浓硫酸的反应:A装置:Cu与浓硫酸反应Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑;装置B装有饱和NaHSO3溶液,作用是贮存多余的二氧化硫气体,装置C收集二氧化硫气体,因二氧化硫能使品红褪色,装置D检验二氧化硫的漂白性,二氧化硫有毒,装置D中试管口放置的棉花中应浸一种液体为氢氧化钠溶液,用浸有NaOH溶液的棉团塞在试管口吸收二氧化硫.
(1)铜是金属,具有还原性,浓硫酸具有强氧化性,加热反应生成硫酸铜、二氧化硫和水
2)当C中气体集满,D中逸出二氧化硫,遇到品红试液会变褪色;
(3)二氧化硫属于酸性气体,能够与氢氧化钠溶液反应,可以用浸有NaOH溶液的棉团塞在试管口吸收二氧化硫;
(4)B中应放置的液体不与二氧化硫反应,也不溶解二氧化硫;
(5)稀硫酸与铜不反应,浓硫酸和铜发生反应随浓度减小,变为稀硫酸后,不能继续和铜发生反应,证明硫酸剩余,需要证明反应后的溶液中存在大量氢离子;
(6)稀硫酸和铜不发生反应,通入氧气后能够反应生成硫酸铜,据此写出反应的化学方程式.
解答 解:(1)铜跟浓硫酸反应,铜具有还原性,浓硫酸具有强氧化性,反应必须加热才能发生,书写化学方程式时注意“浓”字,反应的化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2H2O+SO2↑;
(2)装置E中试管D内盛品红溶液,当C中气体集满,D中有二氧化硫,二氧化硫能和有色物质品红溶液生成无色物质,即品红溶液褪色,
故答案为:品红溶液褪色;
(3)二氧化硫有毒,不能直接排放,氢氧化钠溶液能够与二氧化硫反应,可用浸有NaOH溶液的棉团塞在试管口吸收二氧化硫,反应的离子方程式为:SO2+2OH-=SO32-+H2O,
故答案为:氢氧化钠溶液;在试管口吸收二氧化硫;
(4)装置B的作用是贮存多余的气体,所以B中应放置的液体不能与二氧化硫反应,也不能溶解二氧化硫,而a.饱和Na2SO3溶液和二氧化硫和水生成亚硫酸氢钠、b.酸性KMnO4溶液氧化二氧化硫、C.浓溴水和二氧化硫生成硫酸和氢溴酸,它们都能够与二氧化硫反应,只有d.饱和NaHSO3溶液符合要求,
故答案为:d;
(5)直到反应完毕,最后发现烧瓶中还有一定量的H2SO4和Cu剩余,原因是浓硫酸和铜发生反应随浓度减小,变为稀硫酸后,不能继续和铜发生反应,证明反应后有硫酸剩余,需要证明反应后的溶液中存在大量氢离子,根据金属活动顺序表可知铁能和氢离子反应,稀硫酸与BaC12溶液反应生成硫酸钡,但是不能证明是否含有氢离子;氧化铜与氢离子反应生成铜离子和水,证明溶液中含有氢离子,与饱和Na2CO3溶液反应生成二氧化碳,证明溶液中含有氢离子,所以b不正确,
故答案为:随着反应进行,硫酸被消耗,产物有水生成,所以浓硫酸变成稀硫酸,反应会停止;b;
(6)实验中甲学生向A中反应后溶液中通入一种常见气体单质,使铜片全部溶解且仅生成硫酸铜溶液,该气体单质具有强氧化性,又是常见的,可以为氧气;铜和氧气、稀硫酸发生氧化还原反应,得到硫酸铜和水,反应的化学方程式为:2Cu+O2+2H2SO4═2CuSO4+2H2O,
故答案为:O2;2Cu+O2+2H2SO4═2CuSO4+2H2O.
点评 本题考查了浓硫酸性质的分析应用,生成二氧化硫的还原性、漂白性是分析关键,注意浓硫酸随反应进行变化为稀硫酸不与铜发生反应,题目难度中等.

 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案| A. | Al(OH)3和Al3+ | B. | Al3+、Al(OH)3 和AlO2- | ||
| C. | Al(OH)3 | D. | 全部为AlO2- |
| A. | 氢气 | B. | 氧气 | C. | 二氧化氮 | D. | 一氧化氮 |
| A. | Na | B. | Fe | C. | Cu | D. | Al |
| A. | 氯气具有漂白性和氧化性 | B. | 氨水中含有六种微粒 | ||
| C. | 氯水中含有七种微粒 | D. | 一氧化氮具有还原性 |
| A. | C2H6、C4H8 | B. | C2H6、C3H6 | C. | CH4、C4H8 | D. | CH4、C3H6 |
| A. | 金属钠溶于水:Na+H2O═Na++OH-+H2↑ | |
| B. | 向AlCl3溶液中加入过量氨水:Al3++4OH-═[Al(OH)4]- | |
| C. | 用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O | |
| D. | Cl2溶于水:Cl2+H2O═2H++Cl-+ClO- |
| A. | 同体积、同浓度的NaF和NaCl溶液中,所有离子总数,N(NaCl)>N(NaF);同体积同浓度的Na2CO3和Na2SO4溶液中,所有离子总数,N(Na2CO3)>N(Na2SO4) | |||||||||||
| B. | 以下是某温度下高氯酸、硫酸、硝酸和盐酸在冰醋酸中的电离常数,则在冰醋酸中硫酸的电离方程式可表示为H2SO4?2H++SO42-
| |||||||||||
| C. | 已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中,[c(Na+)-c(F-)]<[c(K+)-c(CH3COO-)] | |||||||||||
| D. | 平衡体系CaCO3(s)?CaO(s)+CO2中仅含有碳酸钙、氧化钙及二氧化碳气体.某时刻,保持温度不变,将容器体积缩小为原来的一半并保持不变,则二氧化碳浓度增大 |