题目内容
某含C、H、O三种元素的未知物A,经燃烧分析实验测定该未知物碳的质量分数为52.16%,氢的质量分数为13.14%,该未知物A的实验式为 .若其摩尔质量为46g/mol,则它的分子式为 .若该未知物A的红外光谱图上发现有O-H键、C-H键和C-O键的振动吸收,该未知物A的结构简式可写为 .
考点:有机物实验式和分子式的确定
专题:有机化学基础
分析:碳的质量分数是52.16%,氢的质量分数是13.14%,则氧元素质量分数是:1-52.16%-13.14%=34.7%,则该物质中碳、氢、氧原子个数之比=
:
:
=4.34%:13,14%:2.17%=2:6:1,据此写出实验式;
根据摩尔质量可知A的相对分子量为46,据此计算出A的分子式;
根据“A的红外吸收光谱表明有C-O键O-H键和C-H键的红外吸收峰”写出A的结构简式.
| 52.16% |
| 12 |
| 13.14 |
| 1 |
| 34.7% |
| 16 |
根据摩尔质量可知A的相对分子量为46,据此计算出A的分子式;
根据“A的红外吸收光谱表明有C-O键O-H键和C-H键的红外吸收峰”写出A的结构简式.
解答:
解:A中含有C、H、O三种元素,碳的质量分数是52.16%,氢的质量分数是13.14%,则氧元素质量分数是:1-52.16%-13.14%=34.7%,则该物质中碳、氢、氧原子个数之比=
:
:
=4.34%:13,14%:2.17%=2:6:1,该未知物A的实验式C2H6O;
A的摩尔质量为46g/mol,则A的相对分子质量为46,实验式C2H6O的式量为46,所以A的分子式为:C2H6O,
A的红外吸收光谱表明有C-O键O-H键和C-H键的红外吸收峰,说明A分子中含有羟基:-OH,则A的结构简式为:CH3CH2OH,
故答案为:C2H6O;C2H6O;CH3CH2OH.
| 52.16% |
| 12 |
| 13.14 |
| 1 |
| 34.7% |
| 16 |
A的摩尔质量为46g/mol,则A的相对分子质量为46,实验式C2H6O的式量为46,所以A的分子式为:C2H6O,
A的红外吸收光谱表明有C-O键O-H键和C-H键的红外吸收峰,说明A分子中含有羟基:-OH,则A的结构简式为:CH3CH2OH,
故答案为:C2H6O;C2H6O;CH3CH2OH.
点评:本题考查了有机物实验式、分子式、结构简式的计算,题目难度中等,注意掌握有机物分子式、结构简式的确定方法,明确质量守恒在确定有机物分子式、结构简式的应用.

练习册系列答案
相关题目
既能与盐酸反应,又能与NaOH溶液反应的是( )
①Na2SO3 ②Al(OH)3 ③NaHCO3 ④Al2O3 ⑤NaHSO4 ⑥Al ⑦(NH4)2CO3 ⑧Na2O2.
①Na2SO3 ②Al(OH)3 ③NaHCO3 ④Al2O3 ⑤NaHSO4 ⑥Al ⑦(NH4)2CO3 ⑧Na2O2.
| A、①②③④ | B、②④⑤⑥⑦ |
| C、②③④⑥⑦⑧ | D、全部 |
下列物质中含有自由移动的Cl-的是( )
| A、KClO3溶液 |
| B、NaCl晶体 |
| C、液态HCl |
| D、熔融的KCl |
某烃通式为CnH2n,该烃可能为( )
| A、丙烷 | B、丙烯 | C、丙炔 | D、苯 |
下列变化不可能通过一步实验直接完成的是( )
| A、Al(OH)3→Al2O3 |
| B、Al2O3→Al(OH)3 |
| C、Al(OH)3→AlCl3 |
| D、AlCl3→Al(OH)3 |

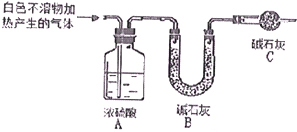 某研究性学习小组做实验做实验时偶然发现,表面擦去氧化膜的镁片可与NaHCO3溶液反应产生大量气体大量气体和白色不溶物,该小组同学通过如下实验,验证产物并探究反应原理.
某研究性学习小组做实验做实验时偶然发现,表面擦去氧化膜的镁片可与NaHCO3溶液反应产生大量气体大量气体和白色不溶物,该小组同学通过如下实验,验证产物并探究反应原理.