题目内容
7.下列说法正确的是( )| A. | 用惰性电极电解含酚酞的饱和食盐水,阳极附近溶液先变红 | |
| B. | 铜的电解精炼过程中,有0.2 mol 电子发生转移时,阳极一定有6.4 g铜溶解 | |
| C. | 将地下钢管与直流电源的正极相连,称为外加电源的阴极保护法 | |
| D. | 在中性环境中,每生成35.6 g铁锈(Fe2O3•H2O),消耗的氧气为6.72 L(标准状况) |
分析 A、电解饱和食盐水时,阳极氯离子放电生成氯气,不会生成氢氧化钠;
B、在电解精炼铜时,阳极上是粗铜,放电的不只是铜,还有比铜活泼的金属杂质;
C、将地下钢管与直流电源的正极相连,则钢管作为阳极,会被腐蚀;
D、根据反应O2+2H2O+4e-=4OH-,结合铁元素守恒可得关系式$\frac{3}{2}$O2~2Fe(OH)3~Fe2O3.H2O计算.
解答 A、用惰性电极电解饱和食盐水时,阳极生成氯气,阴极生成氢气和氢氧根离子,所以阴极生成氢氧化钠,阴极附近溶液先变红,故A错误;
B、在电解精炼铜时,阳极上是粗铜,故阳极上放电的不只是铜,还有比铜活泼的金属杂质,故当转移0.2 mol 电子转移时,阳极上溶解的质量小于6.4,故B错误;
C、将地下钢管与直流电源的正极相连,则钢管作为阳极,会被腐蚀,故C错误;
D、根据反应O2+2H2O+4e-=4OH-,结合铁元素守恒可得关系式$\frac{3}{2}$O2~2Fe(OH)3~Fe2O3.H2O,35.6g铁锈(Fe2O3•H2O)的物质的量为0.2mol,故消耗氧气0.3mol,标况下的体积为0.3×22.4=6.72L,故D正确;
故选D.
点评 本题考查了电解饱和食盐水的原理、阿伏伽德罗常数及氧化还原的有关计算,掌握原理和相关计算公式是解题关键,题目难度中等.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案
相关题目
18. 物质结构与性质包括原子、分子和晶体结构与性质三大内容.请回答下列问题:
物质结构与性质包括原子、分子和晶体结构与性质三大内容.请回答下列问题:
(1)写出基态Fe原子的电子排布图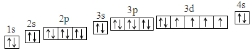 ;第ⅦA族元素原子外围电子排布通式为ns2np5.
;第ⅦA族元素原子外围电子排布通式为ns2np5.
(2)在Al、N、O三种元素中,第一电离能由大到小的排序是N>O>Al;原子半径最大的元素和离子半径最大的元素所组成的物质是AlN(填化学式).
(3)已知几种元素的电负性如下表:
①在上表所列的元素中,在氢化物中H元素化合价显负价的是SiH4、B2H6(填简单氢化物的分子式).
②B3N3H6与苯互为等电子体,其结构式为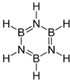 ,能发生加成反应、取代反应(填有机反应类型).
,能发生加成反应、取代反应(填有机反应类型).
③NF3在微电子工业中可作为一种优良的等离子蚀刻气体,其结构与NH3相似,但熔沸点比NH3低很多,其原因是氨分子间能形成氢键,且极性比NF3强,而NF3分子间不能形成氢键.
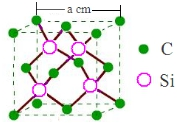
④金刚砂(SiC)硬度仅次于金刚石,可用作砂纸、砂轮的磨料,其晶胞(立方体)如图:则硅原子的杂化类型为sp3,其密度为$\frac{160}{{N}_{A}•{a}^{3}}$g/cm3(以含a的代数式表示).
 物质结构与性质包括原子、分子和晶体结构与性质三大内容.请回答下列问题:
物质结构与性质包括原子、分子和晶体结构与性质三大内容.请回答下列问题:(1)写出基态Fe原子的电子排布图
 ;第ⅦA族元素原子外围电子排布通式为ns2np5.
;第ⅦA族元素原子外围电子排布通式为ns2np5.(2)在Al、N、O三种元素中,第一电离能由大到小的排序是N>O>Al;原子半径最大的元素和离子半径最大的元素所组成的物质是AlN(填化学式).
(3)已知几种元素的电负性如下表:
| H | B | C | N | O | F |
| 2.18 | 2.04 | 2.55 | 3.04 | 3.44 | 3.98 |
| Si | P | S | Cl | ||
| 1.90 | 2.19 | 2.58 | 3.16 |
②B3N3H6与苯互为等电子体,其结构式为
 ,能发生加成反应、取代反应(填有机反应类型).
,能发生加成反应、取代反应(填有机反应类型).③NF3在微电子工业中可作为一种优良的等离子蚀刻气体,其结构与NH3相似,但熔沸点比NH3低很多,其原因是氨分子间能形成氢键,且极性比NF3强,而NF3分子间不能形成氢键.
| 氨 | 三氟化氮 | |
VSEPR模 型 | 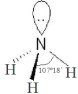 | 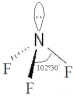 |
| 熔点/℃ | -77.7 | -206.8 |
| 沸点/℃ | -33.5 | -129.0 |
15. 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表:
(1)该反应的平衡常数表达是$\frac{{c}^{2}(N{O}_{2})}{{c}^{2}(NO)•c({O}_{2})}$;800℃反应达到平衡时,NO的物质的量浓度
是0.0035mol/L;升高温度,NO的浓度增大,则该反应是放 (填“放热”或“吸
热”)反应.
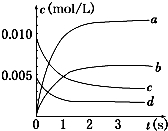
(2)如图中表示NO2变化的曲线是b.用O2表示从0~2s内该反应的平均速率v=0.0015mol/(L•s)或1.5×10-3mol/(L•s).
(3)能说明该反应已达到平衡状态的是bc.
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是c.
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
(5)已知:25℃、101kPa时,①Mn(s)+O2(g)═MnO2(s)△H1=-520kJ/mol
②S(s)+O2(g)═SO2(g)△H2=-297kJ/mol
③Mn(s)+S(s)+2O2(g)═MnSO4(s)△H3=-1065kJ/mol
SO2与MnO2反应生成无水MnSO4的热化学方程式是MnO2(s)+SO2(g)=MnSO4(s)△H=-248kJ/mol.
 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)═2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
是0.0035mol/L;升高温度,NO的浓度增大,则该反应是放 (填“放热”或“吸
热”)反应.
(2)如图中表示NO2变化的曲线是b.用O2表示从0~2s内该反应的平均速率v=0.0015mol/(L•s)或1.5×10-3mol/(L•s).
(3)能说明该反应已达到平衡状态的是bc.
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是c.
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
(5)已知:25℃、101kPa时,①Mn(s)+O2(g)═MnO2(s)△H1=-520kJ/mol
②S(s)+O2(g)═SO2(g)△H2=-297kJ/mol
③Mn(s)+S(s)+2O2(g)═MnSO4(s)△H3=-1065kJ/mol
SO2与MnO2反应生成无水MnSO4的热化学方程式是MnO2(s)+SO2(g)=MnSO4(s)△H=-248kJ/mol.
12.物质的结构决定物质的性质.请回答下列涉及物质结构和性质的问题:
(1)第二周期中,元素的第一电离能处于B与N之间的元素有3种.
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为3d84s2.
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到.乙烯酮分子中碳原子杂化轨道类型是sp2和sp,1mol(C2H5O)3P=O分子中含有的σ键的数目为25NA.
(4)已知固态NH3、H2O、HF的氢键键能和结构如图1:

解释H2O、HF、NH3沸点依次降低的原因单个氢键的键能是(HF)n>冰>(NH3)n,而平均每个分子含氢键数:冰中2个,(HF)n和(NH3)n只有1个,气化要克服的氢键的总键能是冰>(HF)n>(NH3)n.
(5)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能.碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有4个,与碳原子等距离最近的碳原子有12个.已知碳化硅晶胞边长为apm,则晶胞图2中1号硅原子和2号碳原子之间的距离为$\frac{\sqrt{11}a}{4}$pm,碳化硅的密度为$\frac{1.6×1{0}^{32}}{{a}^{3}×{N}_{A}}$g/cm3.
(1)第二周期中,元素的第一电离能处于B与N之间的元素有3种.
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为3d84s2.
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P=O存在下加热脱H2O得到.乙烯酮分子中碳原子杂化轨道类型是sp2和sp,1mol(C2H5O)3P=O分子中含有的σ键的数目为25NA.
(4)已知固态NH3、H2O、HF的氢键键能和结构如图1:
| 物质 | 氢键X-H…Y | 键能kJ.mol-1 |
| (HF)n | D-H…F | 28.1 |
| 冰 | O-H…O | 18.8 |
| (NH3)n | N-H…N | 5.4 |

解释H2O、HF、NH3沸点依次降低的原因单个氢键的键能是(HF)n>冰>(NH3)n,而平均每个分子含氢键数:冰中2个,(HF)n和(NH3)n只有1个,气化要克服的氢键的总键能是冰>(HF)n>(NH3)n.
(5)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能.碳化硅晶胞结构中每个碳原子周围与其距离最近的硅原子有4个,与碳原子等距离最近的碳原子有12个.已知碳化硅晶胞边长为apm,则晶胞图2中1号硅原子和2号碳原子之间的距离为$\frac{\sqrt{11}a}{4}$pm,碳化硅的密度为$\frac{1.6×1{0}^{32}}{{a}^{3}×{N}_{A}}$g/cm3.
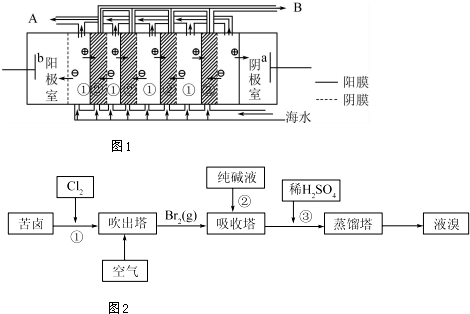
19. 纳米氧化亚铜在水的光解等领域具有极大应用潜能,是极具开发前景的绿色环保光催化剂.目前主要的合成方法有电解法、高温固相法等.
纳米氧化亚铜在水的光解等领域具有极大应用潜能,是极具开发前景的绿色环保光催化剂.目前主要的合成方法有电解法、高温固相法等.
(1)有研究表明阳极氧化法成功制得了Cu2O 纳米阵列,装置如图:该电池的阳极反应方程式为2Cu-2e-+2OH-=Cu2O+H2O离子交换膜为阴(填阳或阴)离子交换膜,铜网应连接电源的正极.
(2)在高温下用甲烷将粉状CuO 还原也可制得Cu2O.
已知:①2Cu(s)+$\frac{1}{2}$O2(g)=Cu2O(s);△H=-169kJ•mol-1
②CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-846.3kJ•mol-1
③Cu(s)+$\frac{1}{2}$O2(g)=CuO(s);△H=-157kJ•mol-1
则该反应的热化学方程式是:8CuO(s)+CH4(g)=4Cu2O(s)+CO2(g)+2H2O(g)△H=-266.3kJ/mol.
(3)在相同的密闭容器中,用等质量的三种纳米Cu2O(用不同方法制得)分别进行催化分解水的实验:2H2O(g)$?_{Cu_{2}O}^{光照}$2H2(g)+O2(g)△H>0.水蒸气浓度随时间t变化如下表所示:
①对比实验的温度:T2>T1(填“>”“<”或“﹦”),原因是因为该反应的正反应方向为吸热方向,升温,平衡正向移动,平衡常数增大,③的平衡常数大于①,说明T2大于T1.
②实验①前20min的平均反应速率 v(O2)=3.5×10-5mol/(L•min)
③比较不同方法制得的Cu2O的催化效果应选用①和②组实验,原因是除催化剂外,其他条件相同.
 纳米氧化亚铜在水的光解等领域具有极大应用潜能,是极具开发前景的绿色环保光催化剂.目前主要的合成方法有电解法、高温固相法等.
纳米氧化亚铜在水的光解等领域具有极大应用潜能,是极具开发前景的绿色环保光催化剂.目前主要的合成方法有电解法、高温固相法等.(1)有研究表明阳极氧化法成功制得了Cu2O 纳米阵列,装置如图:该电池的阳极反应方程式为2Cu-2e-+2OH-=Cu2O+H2O离子交换膜为阴(填阳或阴)离子交换膜,铜网应连接电源的正极.
(2)在高温下用甲烷将粉状CuO 还原也可制得Cu2O.
已知:①2Cu(s)+$\frac{1}{2}$O2(g)=Cu2O(s);△H=-169kJ•mol-1
②CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-846.3kJ•mol-1
③Cu(s)+$\frac{1}{2}$O2(g)=CuO(s);△H=-157kJ•mol-1
则该反应的热化学方程式是:8CuO(s)+CH4(g)=4Cu2O(s)+CO2(g)+2H2O(g)△H=-266.3kJ/mol.
(3)在相同的密闭容器中,用等质量的三种纳米Cu2O(用不同方法制得)分别进行催化分解水的实验:2H2O(g)$?_{Cu_{2}O}^{光照}$2H2(g)+O2(g)△H>0.水蒸气浓度随时间t变化如下表所示:
| 序号 |  | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
②实验①前20min的平均反应速率 v(O2)=3.5×10-5mol/(L•min)
③比较不同方法制得的Cu2O的催化效果应选用①和②组实验,原因是除催化剂外,其他条件相同.
16.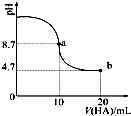 室温下向10mL 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )
室温下向10mL 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )
 室温下向10mL 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )
室温下向10mL 0.1mol•L-1NaOH溶液中加入0.1mol•L-1的一元酸HA,溶液pH的变化曲线如图所示.下列说法正确的是( )| A. | a点所示溶液中c(HA)>c(A-) | |
| B. | 当加入HA溶液10ml时,$\frac{{K}_{W}}{c({H}^{+})}$<1.0×10-7mol•L-1 | |
| C. | a点所示溶液中c(Na+)=c(A-)+c(HA) | |
| D. | b点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA) |
 .
.
 .
. .
.