题目内容
下列说法正确的是( )
| A、苯、乙烯都能因反应而使溴水褪色 |
| B、等质量的甲烷、乙烯、乙炔充分燃烧,消耗氧气的量由少到多 |
C、CH3CH2OH、 、CH3COOH电离出H+的能力由弱到强 、CH3COOH电离出H+的能力由弱到强 |
| D、蔗糖和福尔马林与新制氢氧化铜悬浊液共热,都产生红色沉淀 |
考点:有机化学反应的综合应用
专题:有机反应
分析:A.乙烯能够使溴水褪色,而苯不能与溴水发生反应;
B.烃类物质中,含氢量越大,等质量时燃烧消耗的氧气的量越大;
C.根据乙醇、苯酚、乙酸溶液中能否电离或者电离氢离子能力大小进行判断;
D.福尔马林为甲醛的水溶液,能够与新制的氢氧化铜浊液反应生成红色沉淀,而蔗糖为非还原性糖,不能与氢氧化铜浊液反应.
B.烃类物质中,含氢量越大,等质量时燃烧消耗的氧气的量越大;
C.根据乙醇、苯酚、乙酸溶液中能否电离或者电离氢离子能力大小进行判断;
D.福尔马林为甲醛的水溶液,能够与新制的氢氧化铜浊液反应生成红色沉淀,而蔗糖为非还原性糖,不能与氢氧化铜浊液反应.
解答:
解:A.乙烯能够与溴水发生加成反应而使溴水褪色,而苯不能与溴水发生反应,故A错误;
B.含氢量大小为:甲烷>乙烯>乙炔,含氢量越大,等质量时消耗氧气的量越大,所以等质量的甲烷、乙烯、乙炔充分燃烧,消耗氧气的量由多到少,故B错误;
C.CH3CH2OH为中性, 为极弱的酸性,而CH3COOH为中强酸,所以CH3CH2OH、
为极弱的酸性,而CH3COOH为中强酸,所以CH3CH2OH、 、CH3COOH电离出H+的能力由弱到强,故C正确;
、CH3COOH电离出H+的能力由弱到强,故C正确;
D.蔗糖分子中不含有醛基,不能与新制的氢氧化铜浊液反应生成红色沉淀,故D错误;
故选C.
B.含氢量大小为:甲烷>乙烯>乙炔,含氢量越大,等质量时消耗氧气的量越大,所以等质量的甲烷、乙烯、乙炔充分燃烧,消耗氧气的量由多到少,故B错误;
C.CH3CH2OH为中性,
 为极弱的酸性,而CH3COOH为中强酸,所以CH3CH2OH、
为极弱的酸性,而CH3COOH为中强酸,所以CH3CH2OH、 、CH3COOH电离出H+的能力由弱到强,故C正确;
、CH3COOH电离出H+的能力由弱到强,故C正确;D.蔗糖分子中不含有醛基,不能与新制的氢氧化铜浊液反应生成红色沉淀,故D错误;
故选C.
点评:本题考查了有机物结构与性质,题目难度中等,注意熟练掌握常见有机物的结构与性质,试题能够培养学生灵活应用所学知识的能力.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
有机化学中取代反应范畴很广,下列反应不属于取代反应的是( )
A、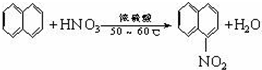 |
B、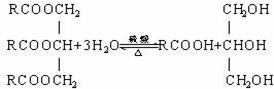 |
C、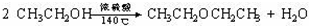 |
D、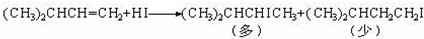 |
已知分解1mol H2O2放出热量98kJ,在含少量I-的溶液中,H2O2分解的机理为:
H2O2+I-→H2O+IO- 慢
H2O2+IO-→H2O+O2+I- 快
下列有关该反应的说法正确的是( )
H2O2+I-→H2O+IO- 慢
H2O2+IO-→H2O+O2+I- 快
下列有关该反应的说法正确的是( )
| A、反应速率与I-的浓度有关 |
| B、IO-也是该反应的催化剂 |
| C、反应活化能等于98kJ?mol-1 |
| D、v(H2O2)=v(H2O)=v(O2) |
下列排列顺序错误的是( )
| A、酸性:H4SiO4<H3PO4<H2SO4<HClO4 |
| B、氢化物的稳定性:CH4<NH3<H2O<HF |
| C、碱性:KOH>Ca(OH)2>Mg(OH)2 |
| D、沸点:HI>HBr>HCl>HF |
下列各选项中,前者属于电解质,后者属于非电解质的是( )
| A、KNO3、酒精 |
| B、盐酸、蔗糖 |
| C、二氧化碳、BaSO4 |
| D、NaOH、氯气 |
下列各组物质中,化学键类型相同,晶体类型也相同的是( )
| A、CH4和H2O |
| B、KCl和HCl |
| C、Cl2和KCl |
| D、SiO2和CO2 |
下列说法中正确的是( )
| A、镀锌铁镀层破损后铁更易被腐蚀 |
| B、当生成物成键释放的总能量大于反应物断键吸收的总能量时,此反应为吸热反应 |
| C、生成物的能量大于反应物的总能量时,反应吸热,△H>0 |
| D、铅蓄电池放电时,Pb作正极,PbO2作负极 |
三氟化硼是平面正三角形因此是非极性分子,推断三氯甲烷(碳原子位于分子结构中心)的结构和分子的极性情况是( )
| A、正四面体,非极性分子 |
| B、平面三角形,非极性分子 |
| C、四面体,极性分子 |
| D、平面三角形,极性分子 |
钠与水反应时的现象与钠的下列性质无关的是( )
| A、钠的熔点低 |
| B、钠的密度比水小 |
| C、钠的硬度小 |
| D、钠与水的反应是显著的放热反应 |