题目内容
填写实验报告:三瓶无色溶液:MgCl2、BaCl2、AlCl3,分别加试剂x有下列现象:
| 实验步骤 | 实验现象 | 结论与化学方程式 |
| 三瓶溶液分别取样,分别加入x试剂.x试剂是 |
(1)有白色沉淀,加入过量x试剂,白色沉淀不消失; (2)先有白色沉淀,加入过量x试剂后,沉淀会消失; (3)无明显现象 |
该物质是 离子方程式是 该物质是 该物质是 |
考点:物质的检验和鉴别的实验方案设计,离子方程式的书写
专题:物质检验鉴别题
分析:MgCl2、AlCl3均与NaOH反应,但氢氧化铝溶于过量的NaOH,氢氧化镁不能,以此鉴别二者,BaCl2与NaOH不反应,以此来解答.
解答:
解:因MgCl2、AlCl3均与NaOH反应,但氢氧化铝溶于过量的NaOH,氢氧化镁不能,以此鉴别二者,BaCl2与NaOH不反应,则试剂x为NaOH,
由现象(1)可知,该物质为MgCl2,离子反应为Mg2++2OH-=Mg(0H)2↓,
由现象(2)可知,该物质为AlCl3,
由现象(3)可知,该物质为BaCl2,
故答案为:
.
由现象(1)可知,该物质为MgCl2,离子反应为Mg2++2OH-=Mg(0H)2↓,
由现象(2)可知,该物质为AlCl3,
由现象(3)可知,该物质为BaCl2,
故答案为:
| 实验步骤 | 实验现象 | 结论与化学方程式 |
| 三瓶溶液分别取样,分别加入x试剂.x试剂是NaOH | (1)有白色沉淀,加入过量x试剂,白色沉淀不消失; (2)先有白色沉淀,加入过量x试剂后,沉淀会消失; (3)无明显现象 |
该物质是MgCl2; 离子方程式是Mg2++2OH-=Mg(0H)2↓; 该物质是AlCl3; 该物质是BaCl2 |
点评:本题考查物质的鉴别和检验,为高频考点,把握物质的性质及现象为解答的关键,侧重物质鉴别的考查,注意氢氧化铝的两性即可解答,题目难度不大.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
某有机物其结构简式为 ,关于该有机物下列叙述正确的是( )
,关于该有机物下列叙述正确的是( )
 ,关于该有机物下列叙述正确的是( )
,关于该有机物下列叙述正确的是( )| A、不能使酸性KMnO4溶液褪色 |
| B、不能使溴水褪色 |
| C、在加热和催化剂作用下,最多能和4mol H2反应 |
| D、一定条件下,能和NaOH醇溶液反应 |
T℃时,CaCO3和CaF2的Ksp分别为1.0×10-12和4.0×10.下列说法正确的是( )
| A、T℃时,两饱和溶液中c(Ca2+):CaCO3>CaF2 |
| B、T℃时,两饱和溶液等体积混合,会析出CaF2固体 |
| C、T℃时,CaF2固体在稀盐酸中的Ksp比在纯水中的Ksp大 |
| D、T℃时,向CaCO3悬浊液中加NaF固体,可能析出CaF2固体 |
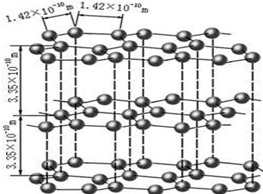
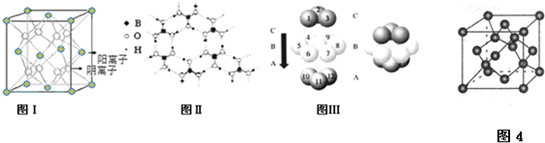
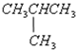 ;⑥石墨;⑦14C;⑧CO2.
;⑥石墨;⑦14C;⑧CO2.
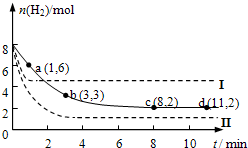 固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+Q(Q>0)某科学实验小组将6mol CO2和8mol H2充入一容积为2L的密闭容器中(温度保持不变),测得H2的物质的量随时间变化如下图中实线所示(图中字母后的数字表示对应的坐标).回答下列问题:
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+Q(Q>0)某科学实验小组将6mol CO2和8mol H2充入一容积为2L的密闭容器中(温度保持不变),测得H2的物质的量随时间变化如下图中实线所示(图中字母后的数字表示对应的坐标).回答下列问题: ,它可通过不同化学反应分别制得B、C、D和E四种物质.
,它可通过不同化学反应分别制得B、C、D和E四种物质.