题目内容
下列物质中,互为同位素的是 (填序号,下同),互为同素异形体的是 ,互为同系物的是 ,互为同分异构体的是 .
①金刚石;②CH4;③12C;④CH3CH2CH2CH3;⑤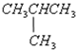 ;⑥石墨;⑦14C;⑧CO2.
;⑥石墨;⑦14C;⑧CO2.
①金刚石;②CH4;③12C;④CH3CH2CH2CH3;⑤
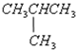 ;⑥石墨;⑦14C;⑧CO2.
;⑥石墨;⑦14C;⑧CO2.考点:芳香烃、烃基和同系物,同位素及其应用,同素异形体,同分异构现象和同分异构体
专题:同系物和同分异构体
分析:由同种元素形成的不同种单质互为同素异形体;
质子数相同,中子数不同的原子互称同位素;
同分异构体是分子式相同,结构式不同的化合物;
结构相似,分子组成上相差1个或者若干个CH2基团的化合物互称为同系物;
根据以上知识进行判断.
质子数相同,中子数不同的原子互称同位素;
同分异构体是分子式相同,结构式不同的化合物;
结构相似,分子组成上相差1个或者若干个CH2基团的化合物互称为同系物;
根据以上知识进行判断.
解答:
解:12C和14C,二者是质子数相同,中子数不同的原子,互为同位素,所以互为同位素的是③⑦;
金刚石和石墨,二者是由碳元素形成的不同种单质,互为同素异形体,互为同素异形体的是①⑥;
CH4和CH3CH2CH2CH3,二者结构相似,分子组成上相差3个CH2基团,属于同系物;互为同系物的是②④;
CH3CH2CH2CH3和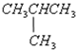 ,二者分子式相同,结构不同,属于同分异构体,所以属于同分异构体的是④⑤;
,二者分子式相同,结构不同,属于同分异构体,所以属于同分异构体的是④⑤;
故答案为:③⑦;①⑥;②④;④⑤.
金刚石和石墨,二者是由碳元素形成的不同种单质,互为同素异形体,互为同素异形体的是①⑥;
CH4和CH3CH2CH2CH3,二者结构相似,分子组成上相差3个CH2基团,属于同系物;互为同系物的是②④;
CH3CH2CH2CH3和
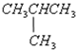 ,二者分子式相同,结构不同,属于同分异构体,所以属于同分异构体的是④⑤;
,二者分子式相同,结构不同,属于同分异构体,所以属于同分异构体的是④⑤;故答案为:③⑦;①⑥;②④;④⑤.
点评:本题考查了同分异构体、同位素、同素异形体、同系物的判断,题目难度不大,明确概念是解本题的关键.

练习册系列答案
相关题目
煤的气化所得气体可用于城市家用燃气.下列选项中的气体均属于家用燃气有效成分的是( )
| A、?CO、H2、N2 |
| B、?CO、CH4、H2 |
| C、?CO、CH4、CO2 |
| D、?CH4、H2、O2 |
下列有关排列顺序正确的是( )
| A、微粒半径:S>O>N |
| B、熔沸点:HF>HBr>HCl |
| C、酸性:H2SO4>HClO4>H2CO3 |
| D、碱性:Al(OH)3>Mg(OH)2>NaOH |

