题目内容
11.已知X、M都是中学教材常见元素,下列对两个离子反应通式的推断中,其中正确的是( )(甲)XO3n-+Xn-+H+→X单质+H2O(未配平);(乙)Mm++mOH-=M(OH)m↓
①若n=1,则XO3n-中X元素为+5价,X位于周期表第ⅤA族
②若n=2,则X最高价氧化物的水化物可能与它的氢化物反应
③若m=1,则M(NO3)m溶液和氨水互滴时的现象可能不同
④若m=2,则在空气中蒸干、灼烧MSO4溶液一定能得到MSO4
⑤若m=3,则MCl3与足量氢氧化钠溶液反应一定生成M(OH)m.
| A. | ②③ | B. | ①③ | C. | ④⑤ | D. | ②④ |
分析 ①n=1,XO3n-中X元素为+5价,常见非金属元素中呈+5价的元素有第ⅤA族(氮、磷)、第ⅤⅡA族(氯、溴、碘)所以符合条件的酸根阴离子主要有:IO3-、ClO3-、BrO3-、NO3-,甲反应为ClO3-+5Cl-+6H+=3Cl2+3H2O,IO3-+5I-+6H+=3I2+3H2O;
②n=2,XO3n-中X元素为+4价,常见非金属元素中碳、硅、硫有+4价,结合通式只有X为硫符合题意,离子方程式为:SO32-+2S2-+6H+=3S↓+3H2O,硫的高价含氧酸为亚硫酸,氢化物为硫化氢;
③m=1,+1价阳离子有:Ag+、Na+、K+等,只有氢氧化银是难溶于水的沉淀;Ag++OH-=AgOH↓;氢氧化银溶于氨水,硝酸银溶液滴入氨水,生成银氨溶液无明显现象;将氨水滴入硝酸银溶液中 产生沉淀,继续滴加沉淀溶解,互滴顺序不同现象不同;
④m=2,硫酸亚铁中+2价铁在空气中易被氧化为+3价,其化学方程式为:FeSO4+2H2O?Fe(OH)2+3H2O;4Fe(OH)2+O2+2H2O=4Fe(OH)3,2Fe(OH)3$\frac{\underline{\;加热\;}}{\;}$Fe2O3+3H2O Fe2O3+3H2SO4=Fe(SO4)3+3H2O 总反应为:12FeSO4+3O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4Fe2(SO4)3,即硫酸亚铁溶液经蒸干、灼烧得到硫酸铁和氢氧化铁混合物;
⑤m=3,常见金属中只有铁、铝符合条件,以此解答该题.
解答 解:①n=1,XO3n中X元素为+5价,常见非金属元素中呈+5价的元素有第ⅤA族(氮、磷)、第ⅤⅡA族(氯、溴、碘)所以符合条件的酸根阴离子主要有:IO3-、ClO3-、BrO3-、NO3-,甲反应为ClO3-+5Cl-+6H+=3Cl2+3H2O,IO3-+5I-+6H+=3I2+3H2O,故①错误;
②n=2,XO3n中X元素为+4价,常见非金属元素中碳、硅、硫有+4价,结合通式只有X为硫符合题意,离子方程式为:SO32-+2S2-+6H+=3S↓+3H2O,硫的最高价含氧酸为硫酸,氢化物为硫化氢,故②正确;
③m=1,+1价阳离子有:Ag+、Na+、K+等,只有氢氧化银是难溶于水的沉淀;Ag++OH-=AgOH↓;氢氧化银溶于氨水,硝酸银溶液滴入氨水,生成银氨溶液无明显现象;将氨水滴入硝酸银溶液中 产生沉淀,继续滴加沉淀溶解,互滴顺序不同现象不同,故③正确;
④m=2,硫酸亚铁中+2价铁在空气中易被氧化为+3价,其化学方程式为:FeSO4+2H2O?Fe(OH)2+3H2O;4Fe(OH)2+O2+2H2O=4Fe(OH)3,2Fe(OH)3$\frac{\underline{\;加热\;}}{\;}$Fe2O3+3H2O Fe2O3+3H2SO4=Fe(SO4)3+3H2O 总反应为:12FeSO4+3O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4Fe2(SO4)3,即硫酸亚铁溶液经蒸干、灼烧得到硫酸铁和氢氧化铁混合物,故④错误;
⑤m=3,常见金属中只有铁、铝符合条件,铝和过量氢氧化钠沉淀会溶解,故⑤错误;,
故选A.
点评 本题考查元素化合物的推断,属于开放性题目,侧重于学生的分析能力的考查,题目综合性较大,需要学生熟练掌握元素化合物知识,难度中等.

| A. | 有机物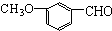 ,有多种同分异构体,其中属于酯且含有苯环结构的共有4种 ,有多种同分异构体,其中属于酯且含有苯环结构的共有4种 | |
| B. | 除去乙烯中混有的甲烷,可将混合气体通过酸性高锰酸钾溶液 | |
| C. | 甲酸分子中有醛基,因此无法区别甲醛溶液和甲酸溶液 | |
| D. | 苯乙烯分子中所有原子可能在一个平面上 |
| A. | 煤的干馏产物主要是各类有机物 | |
| B. | 石油的裂解、分馏和煤的干馏都属于化学变化 | |
| C. | 石油的裂化,说明长链烃在高温条件下可以分解为短链烃 | |
| D. | 煤焦油经过分馏可得到苯、甲苯等,说明煤中含有苯和甲苯 |
| A. | 只有氧化钠 | B. | 只有过氧化钠 | ||
| C. | 氧化钠和过氧化钠 | D. | 无法确定 |
方法Ⅰ:铜铝混合物$→_{充分反应}^{足量溶液A}$测定生成气体的体积
方法Ⅱ:铜铝混合物$→_{充分反应}^{足量B溶液}$测定剩余固体的质量.
| A. | 溶液A和溶液B均可以是盐酸或NaOH溶液 | |
| B. | 实验室中方案Ⅱ更便于实施 | |
| C. | 若溶液B选用浓硝酸,测得铜的质量分数偏大 | |
| D. | 方案一可能产生氢气,方案二可能剩余铜 |
| A. | 1 L 1 mol•L-1的NaCl溶液 | B. | 0.1 L 2 mol•L-1的KCl溶液 | ||
| C. | 0.1 L 1 mol•L-1的MgCl2溶液 | D. | 10 mL 1 mol•L-1的AlCl3溶液 |
Na2CO3•xH2O $\stackrel{加热}{→}$ Na2CO3+x H2O
现有一种碳酸钠晶体(Na2CO3•xH2O),为了测定其组成,某学生在不同温度下给试样加热(温度逐次升高),实验结果记录如下:
坩埚质量32.500g;(坩埚+晶体试样)的质量55.700g.
| 实验次数 | 温度(℃) | 冷却后(坩埚+试样)的质量(g) |
| 1 | T1 | 48.500 |
| 2 | T2 | 44.900 |
| 3 | T3 | 43.100 |
| 4 | T4 | 43.100 |
(2)计算确定碳酸钠晶体(Na2CO3•xH2O )中的x值.(写出计算过程)
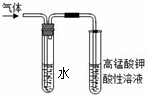 学习卤代烃的性质时,张老师通过实验的方法验证溴乙烷在不同溶剂中与NaOH 反应生成不同的反应产物,请你一起参与他们的探究.
学习卤代烃的性质时,张老师通过实验的方法验证溴乙烷在不同溶剂中与NaOH 反应生成不同的反应产物,请你一起参与他们的探究.