题目内容
19.下列说法正确的是( )| A. | 两种不同元素的原子中,137Cs比131I多6个中子 | |
| B. | 多电子原子中,在离核较远的区域内运动的电子能量较低 | |
| C. | 同主族元素的简单阴离子还原性越强,其氢化物的稳定性越强 | |
| D. | 短周期元素X和Y的原子序数相差2,则X与Y可能同周期,也可能同主族 |
分析 A.Cs与碘的质子数不同;
B.原子核外电子是分层排布的,距离原子核越近能量越低;
C.同主族简单阴离子还原性越强,元素的非金属性越弱,氢化物稳定性与元素金属性一致;
D.短周期元素X、Y的原子序数相差2,可能为同周期的元素,也可能为同一主族元素.
解答 解:A.Cs与碘的质子数分别为55,53,137Cs比131I中子数分别为82、78,故A错误;
B.原子核外电子是分层排布的,距离原子核越近能量越低,所以N层能量最高,故B错误;
C.同主族简单阴离子还原性越强,元素的非金属性越弱,氢化物稳定性与元素金属性一致,则该元素对应的气态氢化物稳定性越弱,故C错误;
D.短周期元素X、Y的原子序数相差2,可能为同周期的元素,如C与O,也可能为同一主族元素,如Li与H,故D正确.
故选D.
点评 本题多角度考查元素周期表与周期律知识,为高考常见题型和高频考点,侧重于基础知识的综合理解与运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
10.下列说法错误的是( )
| A. | 在熔化状态下能导电的化合物一定是离子晶体 | |
| B. | 分子晶体的状态变化只需克服分子间作用力 | |
| C. | 金属键的本质是金属离子与自由电子间的相互作用 | |
| D. | 原子晶体中只存在非极性共价键 |
14. 如图所示,在盛有水的烧杯中倒置一支试管,底部有一枚铁钉,放置数天后观察:
如图所示,在盛有水的烧杯中倒置一支试管,底部有一枚铁钉,放置数天后观察:
铁钉在逐渐生锈,下列说法中不正确的是( )
 如图所示,在盛有水的烧杯中倒置一支试管,底部有一枚铁钉,放置数天后观察:
如图所示,在盛有水的烧杯中倒置一支试管,底部有一枚铁钉,放置数天后观察:铁钉在逐渐生锈,下列说法中不正确的是( )
| A. | 铁钉生锈,铁钉的腐蚀属于电化学腐蚀腐蚀 | |
| B. | 若试管内液面上升,则铁钉发生的是吸氧腐蚀 | |
| C. | 若试管内液面上升,则铁钉发生的是析氢腐蚀 | |
| D. | 若试管内液面下降,则铁钉发生的是析氢腐蚀 |
4.下列说法中正确的是( )
| A. | H2与O2的反应是熵增的放热反应 | |
| B. | 能说明盐酸是强酸的反应:HCl+AgNO3=AgCl↓+HNO3 | |
| C. | 向NaCl和KI的混合溶液中,逐滴加入AgNO3溶液,先产生黄色沉淀,则Ksp(AgCl)<Ksp(AgI) | |
| D. | 配制一定浓度的硫酸铝溶液时,应先加稀硫酸溶解硫酸铝固体,再稀释至所需浓度 |
8.2015年11月世界气候大会再次提出全球变暖的问题.下列物质属于温室气体的是( )
| A. | SO2 | B. | NO2 | C. | O2 | D. | CO2 |
9.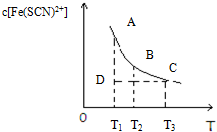 氯化铁和硫氰化钾在溶液中存在下列平衡:Fe3+(aq)+3SCN-(aq)?Fe(SCN)3(aq),某氯化铁和硫氰化钾的混合溶液中,Fe(SCN)3的物质的量浓度与温度T的关系如图所示(曲线上任何一点都表示平衡状态),下列说法不正确的是( )
氯化铁和硫氰化钾在溶液中存在下列平衡:Fe3+(aq)+3SCN-(aq)?Fe(SCN)3(aq),某氯化铁和硫氰化钾的混合溶液中,Fe(SCN)3的物质的量浓度与温度T的关系如图所示(曲线上任何一点都表示平衡状态),下列说法不正确的是( )
 氯化铁和硫氰化钾在溶液中存在下列平衡:Fe3+(aq)+3SCN-(aq)?Fe(SCN)3(aq),某氯化铁和硫氰化钾的混合溶液中,Fe(SCN)3的物质的量浓度与温度T的关系如图所示(曲线上任何一点都表示平衡状态),下列说法不正确的是( )
氯化铁和硫氰化钾在溶液中存在下列平衡:Fe3+(aq)+3SCN-(aq)?Fe(SCN)3(aq),某氯化铁和硫氰化钾的混合溶液中,Fe(SCN)3的物质的量浓度与温度T的关系如图所示(曲线上任何一点都表示平衡状态),下列说法不正确的是( )| A. | FeCl3(aq)与KSCN(aq)反应的热化学反应方程式为:Fe3+(aq)+SCN-(aq)=Fe(SCN)3+(aq)△H>0 | |
| B. | 温度为T1、T2时,反应的平衡常数分别为K1、K2,则K1<K2 | |
| C. | 反应处于D点时,一定有V正>V逆 | |
| D. | A点与B点相比,A点的c(Fe3)+大 |
