题目内容
2.已知核素${\;}_{6}^{12}$C的质量为w g.某元素有两种核素 ${\;}_{Z}^{A}$X和 ${\;}_{Z}^{B}$X,其原子质量分别为a g和b g,它们在自然界中的原子个数百分比分别为 n% 和 m%.(1)${\;}_{Z}^{A}$X的相对原子质量为$\frac{12a}{W}$.
(2)${\;}_{Z}^{B}$X的中子数为B-Z.
(3)元素X的相对原子质量为$\frac{12a}{W}$×n%+$\frac{12b}{W}$×m%.
(4)元素X的近似相对原子质量为A×n%+B×m%.
分析 (1)原子的相对原子质量为该原子的质量与碳原子质量$\frac{1}{12}$的比值;
(2)中子数=质量数-质子数;
(3)元素的相对原子质量等于这种元素的核素的相对原子质量与原子所占的百分数的乘积的和;
(4)元素的近似原子质量为各原子的相对原子量与其百分含量之积的和.
解答 解:(1)原子的相对原子质量为该原子的质量与碳原子质量$\frac{1}{12}$的比值,则${\;}_{Z}^{A}$X相对原子质量为$\frac{ag}{\frac{1}{12}×Wg}$=$\frac{12a}{W}$;
故答案为:$\frac{12a}{W}$;
(2)中子数=质量数-质子数,则${\;}_{Z}^{B}$X的中子数为B-Z;
故答案为:B-Z;
(3)元素的相对原子质量等于这种元素的核素的相对原子质量与原子所占的百分数的乘积的和,则元素的相对原子质量为$\frac{12a}{W}$×n%+$\frac{12b}{W}$×m%;
故答案为:$\frac{12a}{W}$×n%+$\frac{12b}{W}$×m%;
(4)元素的近似原子质量为各原子的相对原子量与其百分含量之积的和,为A×n%+B×m%,故答案为:A×n%+B×m%.
点评 本题考查了原子的构成、相对原子质量的计算,为高频考点,侧重于学生的分析、计算能力的考查,题目难度不大,明确原子的相对原子质量与元素的相对原子质量的区别是解题的关键.

练习册系列答案
相关题目
13.除去下列溶液中的杂质(括号内的物质),下列做法不正确的是( )
| A. | NaCl溶液(BaCl2),加Na2SO4溶液,过滤 | |
| B. | KNO3溶液(AgNO3),加KCl溶液,过滤 | |
| C. | NaCl溶液(I2),加酒精,分液 | |
| D. | KNO3溶液(I2),加四氯化碳,分液 |
10.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下22.4LCCl4含有C-Cl键的数目为4NA | |
| B. | 电解精炼铜时,若转移的电子数为NA个,则阳极减小质量为32g | |
| C. | 电解旅58.5g熔融NaCl,标准状况能产生22.4L氯气、23.0g金属钠 | |
| D. | 己知N2(g)+3H2(g)=2NH3(g)△H=-40.3kJ•mol-1,则在相同条件下通入6molH2和2molN2进行该反应时放出热量小于80.6kJ |
17.下列分子式表示的物质一定是纯净物的是( )
| A. | C5H10 | B. | 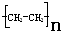 | C. | CH4O | D. | C2H4Cl2 |
7.下列化合物中不可能通过化合反应制得的是( )
①Fe(OH)3②FeCl2③Fel3④SO3⑤CuS⑥NaHCO3.
①Fe(OH)3②FeCl2③Fel3④SO3⑤CuS⑥NaHCO3.
| A. | ③⑤⑥ | B. | ③④⑤⑥ | C. | ③⑤ | D. | ②③⑤ |
14.下列表示对应化学反应的离子方程式正确的是( )
| A. | 向NaClO和NaCl混合溶液中滴入少量FeSO4溶液,反应的离子方程式为:2Fe2++ClO-+2H+═Cl-+2Fe3++H2O | |
| B. | 用少量氨水吸收二氧化硫:SO2+NH3•H2O═HSO3-+NH4+ | |
| C. | 少量CO2通入苯酚钠溶液: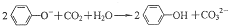 | |
| D. | 向明矾溶液中滴加Ba(OH)2溶液至溶液呈中性:2Al3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓ |
11.下列指定反应的离子方程式正确的是( )
| A. | 将铜插入稀硝酸中:Cu+4H++2NO3-=Cu2++2NO2↑+H2O | |
| B. | 向Fe2(SO4)3溶液中加入过量铁粉:Fe3++Fe=2Fe3+ | |
| C. | 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+3Na+ | |
| D. | 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3﹒H2O=Al(OH)3↓+3NH4+ |
12.说法正确的是( )
| A. | 若1mol Na2O2与足量水反应后产生氧气,理论上转移的电子数为2×6.02×1023 | |
| B. | 0.1mol/L Na2CO3溶液加热后,溶液的pH减小 | |
| C. | 室温下稀释0.1mol/L CH3COOH溶液,溶液的导电能力减弱,因此溶液中所有离子浓度均减小 | |
| D. | 向废水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进Fe3+水解 |

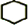 ,名称是环己烷
,名称是环己烷 +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$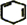 +2NaBr+2H2O.
+2NaBr+2H2O.