题目内容
1.下列叙述正确的是( )| A. | 某主族元素的最高价含氧酸为HnROm,则其气态氢化物一般是H2m-nR | |
| B. | 除第ⅡA族族外,其余各族都有非金属元素 | |
| C. | 同一主族相邻的两种元素的原子序数之差可能为16 | |
| D. | 同一短周期元素的原子半径从左到右逐渐减小 |
分析 A、先判断酸中的化合价,再根据主族元素的最高正价与最低负价的绝对值之和为8,判断最低负价,从而判断氢化物的化学式;
B、过渡元素没有非金属;
C、同一主族的两种元素的原子序数之差为2、8、8、18、18、32等;
D、短周期元素同一周期中,原子半径随核电荷数的增加而减小;
解答 解:A、最高价含氧酸为HnROm,根据分子中各元素化合价的代数和为0判断,其最高价为+(2m-n),再根据主族元素的最高正价与最低负价的绝对值之和为8,所以其最低负价为:(2m-n)-8,所以其氢化物的化学式一般为H8+n-2mR,故A错误;
B、过渡元素没有非金属,故B错误;
C、同一主族相邻的两种元素的原子序数之差为2、8、8、18、18、32等,不可能为16,故C错误;
D、短周期元素同一周期中,原子半径随核电荷数的增加而减小,故D正确.
点评 本题考查了原子结构和元素性质,根据物质的性质、原子结构结合元素周期律分析解答,A为易错选项,要分析不同周期元素,题目难度不大.

练习册系列答案
相关题目
11.下列物质中既含有离子键,又含有共价键的是( )
| A. | KCl | B. | PCl3 | C. | NH3•H2O | D. | Na2O2 |
16.下列选项属于官能团异构的是( )
| A. | CH3CH2 CH2CH3和CH3CH(CH3)2 | B. | CH2=C(CH3)2和CH3CH=CHCH3 | ||
| C. | CH3CH2OH和CH3OCH3 | D. | CH3CH2COOH 和CH3COOCH2CH3 |
6.下列描述正确的是( )
| A. | 伴随有能量变化的物质变化都是化学变化 | |
| B. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 | |
| C. | 已知相同条件下2SO2(g)+O2(g)?2SO3(g)△H1,反应2SO2(s)+O2(g)?2SO3(g)△H2,则△H1>△H2 | |
| D. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,若将含0.5 mol H2SO4的浓H2SO4与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
10.已知:A(g)+2B(g)═C(g)+D(g)△H=a kJ•mol-1(a<0),下列说法正确的是( )
| A. | A(g)的能量一定高于C(g)的能量 | |
| B. | 该反应不需要加热 | |
| C. | 1 mol A(g)和2 mol B(g)的总能量高于1 mol C(g)的能量 | |
| D. | 该反应表示:1 mol A(g)和2 mol B(g)在一定条件下反应放出的热量为a kJ |
11.下列化学用语书写正确的是( )
| A. | 丙酸的结构简式:CH3CH2COOH | B. | 甲烷的结构式:CH4 | ||
| C. | 乙烯的结构简式:CH2CH2 | D. | 乙醇的结构式: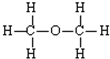 |
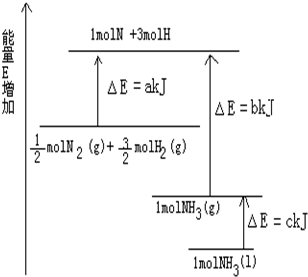 已知化学反应N2+3H2═2NH3的能量变化如图所示,
已知化学反应N2+3H2═2NH3的能量变化如图所示,